
某溶液可能含有Na+、Fe3+、Br﹣、I﹣、HCO3﹣、SO32﹣、NO3﹣等离子①向该溶液中滴加氯水,无气泡产生,溶液呈橙色;②向橙色溶液中加入BaCl2溶液产生白色沉淀;③向橙色溶液中滴加淀粉溶液未变蓝,则在该溶液中肯定存在的离子组是
A.Na+、I﹣、SO32﹣ B.Na+、Br﹣、SO32﹣
C.Fe3+、Br﹣、NO3﹣ D.Na+、Br﹣、NO3﹣
 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案科目:高中化学 来源: 题型:
现有50 g 5 %的硫酸铜溶液,要使其溶液浓度提高至10 %,应该采取措施有:
(1)可蒸发水 g。
(2)加入12.5 %的硫酸铜溶液 g。
(3)加入无水硫酸铜粉末 g。
(4)加入蓝矾晶体 g。
查看答案和解析>>
科目:高中化学 来源: 题型:
下表各组物质中,物质之间不可能实现如图所示转化的是
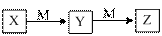
| 选项 | X | Y | Z | M |
| A | NH3 | NO | NO2 | O2 |
| B | Cl2 | FeCl3 | FeCl2 | Fe |
| C | Al | Al(OH)3 | NaAlO2 | NaOH |
| D | NaOH | Na2CO3 | NaHCO3 | CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在指定溶液中一定能大量共存的离子组是
A.1.0mol·L-1KNO3溶液:H+、Fe2+、Cl-、SO42-
B.pH=1的溶液:NH4+、Al3+、SO42-、Br-
C.c(ClO-)=1.0mol·L-1的溶液:Na+、SO32-、S2-、Cl-
D.与铝反应产生H2的溶液中:Na+、Mg2+、HCO3-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
解热镇痛药贝诺酯的合成路线如下:
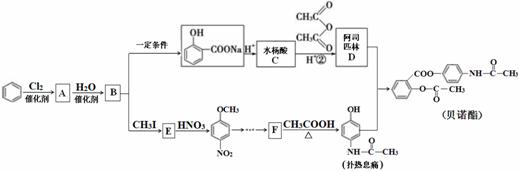
请回答下列问题:
(1)A→B的反应类型为_____________;B→E的另一产物是________。
(2)X是水杨酸的同分异构体,X中含有苯环,属于酯类,遇FeCl3溶液显紫色。则X 的结构简式为_____________(任写一种)。
(3)F中官能团的名称为________________。1mol扑热息痛与足量NaOH溶液反应,消耗NaOH的物质的量为__________。
(4)生成贝诺酯的化学方程式为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
氨氧化法是工业生产中制取硝酸的主要途径,某同学用该原理在实验室探究硝酸的制备和性质,设计了如下图所示的装置。
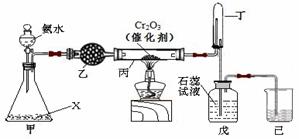
(1)若分液漏斗中氨水的浓度为9.0mol·L-1,配制该浓度的氨水100mL,用到的玻璃仪器有100mL容量瓶、烧杯、玻璃棒、 。
(2)甲装置不需要加热即能同时产生氨气和氧气,烧瓶内固体X的名称为 。
(3)乙装置的作用是 ;写出受热时丙装置发生反应的化学方程式为 。
(4)当戊中观察到 现象,则说明已制得硝酸。某同学按上图组装仪器并检验气密性后进行实验,没有观察到此现象,请分析实验失败的可能原因 。如何改进装置 。
(5)改进后待反应结束,将丁装置倒立在盛水的水槽中,会观察到的现象是 ;为测定试管丁内硝酸溶液的浓度,从中取10mL溶液于锥形瓶中,用0.1 mol·L-1的NaOH溶液滴定。滴定前发现滴定管尖嘴处有少量气泡,请选择排出气泡的正确操作是 。
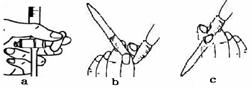
查看答案和解析>>
科目:高中化学 来源: 题型:
硝酸铜是制备Cu—Zn—Al系催化剂的重要原料,制取硝酸铜现有三种设计方案可供选用:
①Cu与稀硝酸反应制取:3Cu+8HNO3(稀)===3Cu(NO3)2+2NO↑+4H2O
②Cu与浓硝酸反应制取:Cu+4HNO3(浓)===Cu(NO3)2+2NO2↑+2H2O
③通氧气于铜屑与稀硝酸的体系中制取:2Cu+4HNO3+O2===2Cu(NO3)2+2H2O
下列说法正确的是 ( )
A.制取相同量的硝酸铜需硝酸的量③最多
B.制取相同量的硝酸铜①产生的有毒气体比②多
C.三种方案中硝酸的利用率③>①>②
D.三种方案的反应都可以在铁制容器中进行
查看答案和解析>>
科目:高中化学 来源: 题型:
某学习小组用下图装置测定镁铝合金中铝的质量分数和铝的相对原子质量。
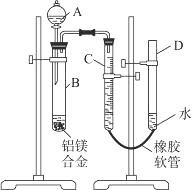
(1)A中试剂为______________。
(2)实验前,先将铝镁合金在稀酸中浸泡片刻,其目的是____________________________。
(3)检查气密性,将药品和水装入各仪器中,连
接好装置后,需进行的操作还有:①记录C的液面
位置;②将B中剩余固体过滤、洗涤、干燥,称重;
③待B中不再有气体产生并恢复至室温后,记录C的液面位置;
④由A向B中滴加足量试剂。
上述操作的顺序是___________(填序号);在进行操作③时记
录C的液面位置时,除视线平视外,还应_ 。
(4)B中发生反应的化学方程式为_________________________________________________。
(5)若实验用铝镁合金的质量为a g,测得氢气体积为b mL(已换算为标准状况),B中剩余固体的质量为c g,则铝的相对原子质量为_______________。
(6)实验过程中,若未洗涤过滤所得的不溶物,则测得铝的质量分数将________(填“偏大”、“偏小”、“无影响”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com