
下列说法正确的是
A.根据反应3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O可知:反应中HNO3表现酸性和氧化性
B.根据反应H3PO3+2NaOH(足量)=Na2HPO3+2H2O可知:H3PO3属于三元酸
C.根据反应5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O可知:用酸性KMnO4溶液可检验绿矾(FeSO4·7H2O)是否变质
D.根据反应CuSO4+H2S=CuS↓+H2SO4可知:H2S的酸性比H2SO4强
科目:高中化学 来源:2014-2015学年天津市高三四月考化学试卷(解析版) 题型:选择题
下列离子方程式正确的是
A.已知电离平衡常数:H2CO3>HClO>HCO3—,向NaClO溶液中通入少量CO2:2ClO—+CO2+H2O=2HClO+CO32—
B.向硫酸氢钠溶液中滴加Ba(OH)2至中性:H++SO42-+Ba2++ OH-=BaSO4↓+ H2O
C.Fe(NO3)3溶液中加入过量的HI溶液:2Fe3+ + 2I-=2Fe2+ + I2
D.硫氢根离子的电离方程式:HS-+H2O H3O++S2-[
H3O++S2-[
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省高三4月过程性检测理综化学试卷(解析版) 题型:简答题
(17分)运用化学反应原理研究碳、氮、硫元素及其化合物有重要意义。
(1)已知一定量的C单质能在O2(g)中燃烧,其可能的产物及能量关系如图所示: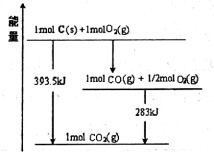
写出CO2(g)与C(s)反应生成CO(g)的热化学方程式_______________________。
(2)汽车尾气净化过程中发生反应2NO(g)+2CO(g) N2+2CO2(g) △H<0。一定条件下,向某密闭恒容容器中按体积比1:l充入44.8L(标准状况)NO和CO混合气体,发生上述反应,某同学根据反应过程中的有关数据绘制了如图所示曲线。
N2+2CO2(g) △H<0。一定条件下,向某密闭恒容容器中按体积比1:l充入44.8L(标准状况)NO和CO混合气体,发生上述反应,某同学根据反应过程中的有关数据绘制了如图所示曲线。
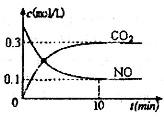
①下列关于上述反应过程的叙述正确的是 ________(填写字母代号)。
A.其它条件不变,加入催化剂,△H的值不变
B.及时除去二氧化碳,反应的正反应速率加快
C.NO、CO、N2、CO2浓度均不再变化,说明平衡未发生移动
D.混合气体的平均相对分子质量不再改变,证明反应达到化学平衡状态
②前10min内CO的平均反应速率为______,达平衡时NO的转化率为_____,能使上述平衡体系中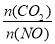 增大的措施有__________(任写一条)。
增大的措施有__________(任写一条)。
(3)已知弱电解质在水中的电离平衡常数(25℃)如下表(单位省略):
弱电解质 | H2CO3 | H2SO3 | NH3·H2O |
电离平衡常数 | Ka1=4.2×10-7 Ka2=5.6×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 | Kb=1.7×10-5 |
①室温条件下。用敞口容器加热氨水一段时间,恢复至室温后,溶液中水的电离程度比加热前_______(填写“增大”、“减小”或“不变”)了.
②常温下,0.1 mo1·L-1(NH4)2SO4溶液呈_____(填“酸”、“中”、“碱”)性。
③常温下,测得某碳酸饮料的pH=6,则该饮料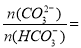 ________。
________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年宁夏银川一中高三第二次模拟考试 理综化学试卷(解析版) 题型:选择题
下表所示为部分短周期元素的原子半径及主要化合价,根据表中信息判断下列叙述不正确的是
元素代号 | A | B | C | D | E | F | G |
原子半径/nm | 0.182 | 0.160 | 0.089 | 0.143 | 0.102 | 0.099 | 0.071 |
主要化合价 | +1 | +2 | +2 | +3 | +6.-2 | -1 | -1 |
A.气态氢化物的稳定性HG>HF>H2E
B.B2+、D3+、E2-、G-四种离子的核外电子排布相同
C.A、E元素与氧元素可以形成三种常见的含氧酸盐
D.C元素的原子最外层电子数等于电子层数
查看答案和解析>>
科目:高中化学 来源:2014-2015学年吉林省高三上学期第五次模拟考试理综化学试卷(解析版) 题型:简答题
(13分)运用化学反应原理研究碳、氮的单质及其化合物的反应对缓解环境污染、能源危机具有重要意义。
(1)用活性炭还原法可以处理氮氧化物。某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g) N2(g)+CO2(g) △H=Q kJ/mol。在T1℃时,反应进行到不同时间(min)测得各物质的浓度(mol/L)如下:
N2(g)+CO2(g) △H=Q kJ/mol。在T1℃时,反应进行到不同时间(min)测得各物质的浓度(mol/L)如下:
浓度 | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
①0~10min内,NO的平均反应速率v(NO)=______,T1℃时,该反应的平衡常数K= ;
②30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是______(填字母编号)。
a.通入一定量的NO b.加入一定量的活性炭
c.加入合适的催化剂 d.适当缩小容器的体积
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为3:1:1,则Q______0(填“>”或“<”)。
④在恒容条件下,能判断该反应一定达到化学平衡状态的依据是______(填选项编号)。
a.单位时间内生成2nmol NO(g)的同时消耗nmol CO2(g)
b.混合气体的平均相对分子质量不再发生改变
c.混合气体的密度不再发生改变
d.反应体系的压强不再发生改变
(2)某研究小组在实验室用某新型催化剂对CO、NO催化转化进行研究,测得NO转化为N2的转化率随温度、CO混存量的变化情况如下图所示,利用以下反应:
NO+CO N2+CO2(有CO) 2NO
N2+CO2(有CO) 2NO N2+O2(无CO)
N2+O2(无CO)
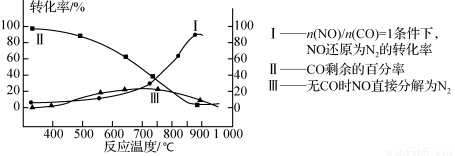
①若不使用CO,温度超过775 ℃,发现NO的分解率降低,其可能的原因为 ;在n(NO)/n(CO)=1的条件下,应控制最佳温度在 左右。
②用CxHy(烃)催化还原NOx也可消除氮氧化物的污染。写出C2H6与NO2发生反应的化学方程式 。
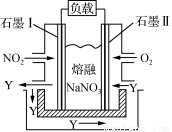
(3)以NO2、O2、熔融NaNO3组成的燃料电池装置如下图所示,在使用过程中石墨Ⅰ电极反应生成一种氧化物Y,则该电极反应式为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省长沙市高三5月一模化学试卷(解析版) 题型:简答题
(17分)汽车尾气中的主要污染物是NO和CO。为减轻大气污染,人们提出通过以下反应来处理汽车尾气:
(1)2NO(g)+2CO(g) 2CO2(g)+N2(g) △H=-746.5KJ/mol (条件为使用催化剂)
2CO2(g)+N2(g) △H=-746.5KJ/mol (条件为使用催化剂)
已知:2C (s)+O2(g) 2CO(g) △H=-221.0KJ/mol
2CO(g) △H=-221.0KJ/mol
C (s)+O2(g) CO2(g) △H=-393.5KJ/mol
CO2(g) △H=-393.5KJ/mol
则N2(g)+O2(g)=2NO(g) △H= kJ·mol-1。
(2)T℃下,在一容积不变的密闭容器中,通入一定量的NO和CO,用气体传感器测得不同时间NO和CO的浓度如下表
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
C(NO)10-4 mol/L | 10.0 | 4.50 | C1 | 1.50 | 1.00 | 1.00 |
C(NO)10-3 mol/L | 3.60 | 3.05 | C2 | 2.75 | 2.70 | 2.70 |
则c1合理的数值为 (填字母标号)。
A.4.20 B.4.00 C.3.50 D.2.50
(3)研究表明:在使用等质量催化剂时,增大催化剂的比表面积可提高化学反应速率。根据下表设计的实验测得混合气体中NO的浓度随时间t变化的趋势如下图所示:
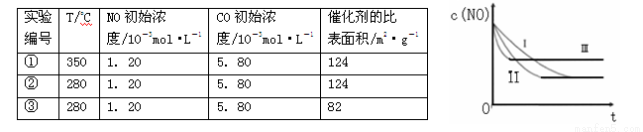
则曲线Ⅰ对应的实验编号依次为 。
(4)将不同物质的量的H2O(g)和CO(g)分别通入体积为2L的恒容密闭容器中,进行反应:H2O(g)+CO(g) CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
H2O | CO | CO | H2 | |||
① | 650 | 2 | 4 | 2.4 | 1.6 | 5 |
② | 900 | 1 | 2 | 1.6 | 0.4 | 3 |
③ | 900 | a | b | c | d | t |
①实验组①中以v(CO2)表示的反应速率为 ,温度升高时平衡常数会 (填“增大”、“减小”或“不变”)。
②若a=2,b=1,则c= ,达平衡时实验组②中H2O(g)和实验组③中CO的转化率的关系为
α2 (H2O) α3 (CO)(填“<”、“>”或“=”)。
(5)CO分析仪的传感器可测定汽车尾气是否符合排放标准,该分析仪的工作原理类似于燃料电池,其中电解质是氧化钇(Y2O3)和氧化锆(ZrO2)晶体,能传导O2-。
①则负极的电极反应式为________________。
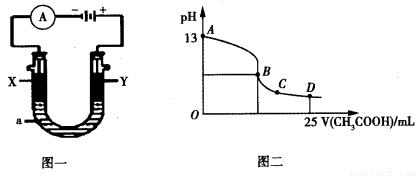
②以上述电池为电源,通过导线连接成图一。若X、Y为石墨,a为2L 0.1mol/L KCl溶液,写出电解总反应的离子方程式 。电解一段时间后,取25mL上述电解后的溶液,滴加0.4mol/L醋酸得到图二曲线(不考虑能量损失和气体溶于水,溶液体积变化忽略不计)。根据图二计算,上述电解过程中消耗一氧化碳的质量为__________g。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省长沙市高三5月一模化学试卷(解析版) 题型:选择题
洋蓟素是一种新结构类型的抗乙型肝炎病毒和抗艾滋病病毒的化合物,其结构如图所示,有关洋蓟素的说法正确的是
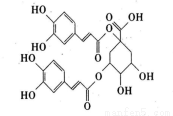
A.洋蓟素的化学式为C25H22O12
B.—定条件下能发生酯化和消去反应
C.1mol洋蓟素最少可有14mol原子共平面
D.1 mol洋蓟素最多可消耗9mol NaOH和6mol Br2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省等高三下学期期中四校联考化学试卷(解析版) 题型:选择题
(A)下列分子中,VSEPR模型名称和分子立体构型名称相同,且分子中各原子最外层都满足8电子稳定结构的是
A.CH4 B.PCl3 C.SiCl4 D.XeF4
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省哈尔滨市高三二模考试理综化学试卷(解析版) 题型:简答题
(17分)铜、铝、硫及其它们的化合物应用广泛,如Cu可用作催化剂、制作印刷电路铜板等。
Ⅰ.铜的冶炼:工业上以辉铜矿为原料,采用火法熔炼工艺生产铜。
火法炼铜的方程式为: ,该工艺的中间过程会发生反应2Cu20+辉铜矿 6Cu+ m↑,若反应每生成5.6 L(标准状况下)m气体.则转移电子的物质的量为 。
6Cu+ m↑,若反应每生成5.6 L(标准状况下)m气体.则转移电子的物质的量为 。
Ⅱ.粗铜精炼:利用电解法可将含有Fe、Zn、Ag、Pt等杂质的粗铜提纯,下列叙述正确的是 。
A.电解时以精铜作阳极
B.电解时阴极发生氧化反应
C.粗铜连接电源负极,其电极反应是Cu一2e—=Cu2+
D.电解后.电解槽底部会形成含少量Ag、Pt等金属的阳极泥
E.整个过程溶液中的Cu2+浓度减少
Ⅲ.铜及其化合物的性质探究:
将洁净的铜丝放在火焰上加热.并趁热插入到乙醇中,铜丝表面的现象为 ,
发生的反应为 。
Ⅳ.无水氯化铝是一种重要的化工原料。利用明矾石:K2SO4·A12(SO4)3·2A1203·6H20]制备无水氯化铝的流程如下:
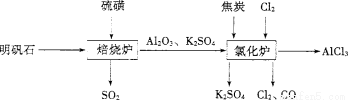
(1)验证焙烧炉产生的气体含有SO2的方法是 。
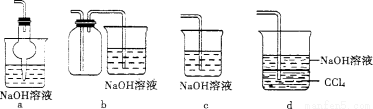
(2)吸收焙烧炉中产生的S02,下列装置合理的是 (填代号)。
(3)氯化炉中发生反应的化学反应方程式为 。
(4)生产氯化铝的过程中会产生SO2、Cl2等大气污染物,若将二者按照一定比例通入水中可减少或消除污染。试设计简单实验检验二者是否恰好完全反应。(简要捕述实验步骤、现象和结论) 。
仪器自选;可供选择试剂如下:①滴加酚酞的氢氧化钠溶液 ②氯化亚铁溶液 ③硫氰化钾溶液 ④品红溶液
(5)某实验小组设计了电化学方法进行二氧化硫的回收利用。利用电化学法将尾气中的SO2气体转化为 氮肥硫酸铵,模拟装置如图:
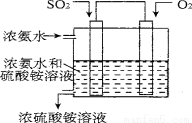
试写出SO2气体发生的电极反应式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com