

 FµÄŌ×Ó½į¹¹Ź¾ŅāĶ¼ĪŖ
FµÄŌ×Ó½į¹¹Ź¾ŅāĶ¼ĪŖ £®
£®·ÖĪö ÓÉŌŖĖŲŌŚÖÜĘŚ±ķÖŠĪ»ÖĆ£¬æÉÖŖAĪŖĒā£¬BĪŖĢ¼£¬CĪŖµŖ£¬DĪŖŃõ£¬EĪŖNa£¬FĪŖCl£®
£Ø1£©DÓėEŅŅ1£ŗ1µÄŌ×ÓøöŹż±ČŠĪ³ÉµÄ»ÆŗĻĪļĪŖNa2O2£¬ÓÉÄĘĄė×Ó¹żŃõøłĄė×Ó¹¹³É£»FĪŖCl£¬Ō×ÓŗĖĶāÓŠ17øöµē×Ó£¬ÓŠ3øöµē×Ó²ć£¬ø÷²ćµē×ÓŹżĪŖ2”¢8”¢7£»
£Ø2£©B”¢DŠĪ³ÉµÄ»ÆŗĻĪļCO2£¬ŹōÓŚ¹²¼Ū»ÆŗĻĪļ£»A”¢C”¢FČżÖÖŌŖĖŲŠĪ³ÉµÄ»ÆŗĻĪļNH4ClŹōÓŚĄė×Ó»ÆŗĻĪļ£»
£Ø3£©»ÆŗĻĪļ¼×”¢ŅŅÓÉH”¢C”¢O”¢NaÖŠµÄČżÖÖ»ņĖÄÖÖ×é³É£¬ĒŅ¼×”¢ŅŅµÄĖ®ČÜŅŗ¾ł³Ź¼īŠŌ£¬ĒŅ¶žÕßæÉŅŌ·¢Éś·“Ó¦£¬Ó¦ŹĒNaOHÓėNaHCO3£»
£Ø4£©ĖłÓŠŌŖĖŲÖŠĒāŌ×Ó°ė¾¶×īŠ”£¬Ķ¬ÖÜĘŚ×Ō×ó¶ųÓŅŌ×Ó°ė¾¶¼õŠ”£¬Ķ¬Ö÷×å×ŌÉĻ¶ųĻĀŌ×Ó°ė¾¶Ōö“ó£»
£Ø5£©Ķ¬ÖÜĘŚ×Ō×ó¶ųÓŅŌŖĖŲ·Ē½šŹōŠŌŌöĒ棬æÉŅŌĄūÓĆ×īøß¼Ūŗ¬ŃõĖįÖŠĒæĖįÖʱøČõĖį½ųŠŠŃéÖ¤£®
½ā“š ½ā£ŗÓÉŌŖĖŲŌŚÖÜĘŚ±ķÖŠĪ»ÖĆ£¬æÉÖŖAĪŖĒā£¬BĪŖĢ¼£¬CĪŖµŖ£¬DĪŖŃõ£¬EĪŖNa£¬FĪŖCl£®
£Ø1£©DÓėEŅŅ1£ŗ1µÄŌ×ÓøöŹż±ČŠĪ³ÉµÄ»ÆŗĻĪļĪŖNa2O2£¬ÓÉÄĘĄė×Ó¹żŃõøłĄė×Ó¹¹³É£¬µē×ÓŹ½ĪŖ £»FĪŖCl£¬Ō×ÓŗĖĶāÓŠ17øöµē×Ó£¬Ō×Ó½į¹¹Ź¾ŅāĶ¼ĪŖ
£»FĪŖCl£¬Ō×ÓŗĖĶāÓŠ17øöµē×Ó£¬Ō×Ó½į¹¹Ź¾ŅāĶ¼ĪŖ £¬
£¬
¹Ź“š°øĪŖ£ŗ £»
£» £»
£»
£Ø2£©B”¢DŠĪ³ÉµÄ»ÆŗĻĪļCO2£¬ŹōÓŚ¹²¼Ū»ÆŗĻĪļ£¬ŗ¬ÓŠ¹²¼Ū¼ü£»A”¢C”¢FČżÖÖŌŖĖŲŠĪ³ÉµÄ»ÆŗĻĪļNH4ClŹōÓŚĄė×Ó»ÆŗĻĪļ£¬
¹Ź“š°øĪŖ£ŗ¹²¼Ū£»Ąė×Ó£»
£Ø3£©»ÆŗĻĪļ¼×”¢ŅŅÓÉH”¢C”¢O”¢NaÖŠµÄČżÖÖ»ņĖÄÖÖ×é³É£¬ĒŅ¼×”¢ŅŅµÄĖ®ČÜŅŗ¾ł³Ź¼īŠŌ£¬ĒŅ¶žÕßæÉŅŌ·¢Éś·“Ó¦£¬Ó¦ŹĒNaOHÓėNaHCO3£¬·“Ó¦Ąė×Ó·½³ĢŹ½ĪŖ£ŗHCO3-+OH-=CO32-+H2O£¬
¹Ź“š°øĪŖ£ŗHCO3-+OH-=CO32-+H2O£»
£Ø4£©ĖłÓŠŌŖĖŲÖŠĒāŌ×Ó°ė¾¶×īŠ”£¬Ķ¬ÖÜĘŚ×Ō×ó¶ųÓŅŌ×Ó°ė¾¶¼õŠ”£¬Ķ¬Ö÷×å×ŌÉĻ¶ųĻĀŌ×Ó°ė¾¶Ōö“󣬹ŹĄė×Ó°ė¾¶£ŗNa£¾N£¾O£¾H£¬
¹Ź“š°øĪŖ£ŗNa£¾N£¾O£¾H£»
£Ø5£©Ķ¬ÖÜĘŚ×Ō×ó¶ųÓŅŌŖĖŲ·Ē½šŹōŠŌŌöĒ棬¹Ź·Ē½šŹōŠŌC£¼N£¬æÉŅŌĄūÓĆ×īøß¼Ūŗ¬ŃõĖįÖŠĒæĖįÖʱøČõĖį½ųŠŠŃéÖ¤£¬·“Ó¦·½³ĢŹ½ĪŖ£ŗNa2CO3+2HNO3=2NaNO3+CO2”ü+H2O£¬
¹Ź“š°øĪŖ£ŗČõ£»Na2CO3+2HNO3=2NaNO3+CO2”ü+H2O£®
µćĘĄ ±¾Ģāæ¼²éŌŖĖŲÖÜĘŚ±ķÓėŌŖĖŲÖÜĘŚĀÉÓ¦ÓĆ£¬ÄŃ¶Č²»“ó£¬ÓŠĄūÓŚ»ł“”ÖŖŹ¶µÄ¹®¹Ģ£¬×¢Ņā½šŹōŠŌ”¢·Ē½šŹōŠŌĒæČõ±Č½ĻŹµŃéŹĀŹµ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ĮłÖÖŅ»äå“śĪļµÄČŪµć/”ćC | 234 | 206 | 213 | 204 | 214 | 205 |
| ¶ŌÓ¦¶ž¼×±½µÄČŪµć/”ćC | 13 | -54 | -27 | -54 | -27 | -54 |
| A£® | 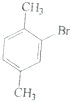 | B£® | 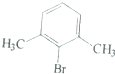 | C£® | 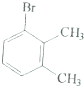 | D£® | 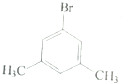 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | C£Øs£©+O2£Øg£©ØTCO2£Øg£©”÷H=-393.5kJ/mol | B£® | C£Øs£©+$\frac{1}{2}$O2£Øg£©ØTCO£Øg£©”÷H=-110.5kJ/mol | ||
| C£® | 2H2£Øg£©+O2£Øg£©ØT2H2O£Øl£©”÷H=-571.6kJ/mol | D£® | H2£Øg£©+$\frac{1}{2}$O2£Øg£©ØTH2O£Øg£©”÷H=-241.8kJ/mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | pH=7µÄČÜŅŗ | B£® | c£ØH+£©=c£ØOH£©=10-6mol/LČÜŅŗ | ||
| C£® | Ź¹·ÓĢŖŹŌŅŗ³ŹĪŽÉ«µÄČÜŅŗ | D£® | ČĪŗĪŃĪČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | äåŅŅĶé | B£® | ŅŅ“¼ | C£® | ÓĶĖį | D£® | ŅŅĖįŅŅõ„ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2-ŅŅ»łĪģĶé | B£® | 1£¬2-¶ž¼×»ł¶”Ķé | ||
| C£® | 2£¬2£¬4-Čż¼×»łĪģĶé | D£® | 2Ņ»ŅŅ»łŅ»3Ņ»¼×»łŅŃĶé |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĘųĢå·Ö×ÓµÄĦ¶ūÖŹĮæ | B£® | Ī¢Į£±¾ÉķµÄ“óŠ” | ||
| C£® | Ī¢Į£µÄÖŹĮæ | D£® | Ī¢Į£¼äµÄĘ½¾ł¾ąĄė |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com