
 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学键 | C-H | C=C | C-C | H-H |
| 键能(kJ•mol-1) | 414.4 | 615.3 | 347.4 | 435.5 |
| A. | +288.8kJ/mo1 | B. | -703.4 kJ/mo1 | C. | +125.4kJ/mo1 | D. | -125.4 kJ/mo1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
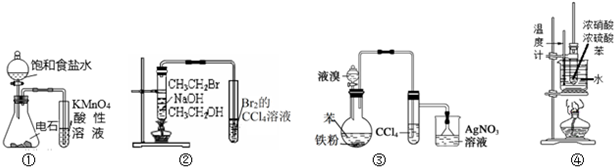
| A. | 装置①可用于检验乙炔的还原性 | |
| B. | 装置②可以证明CH3CH2Br发生消去反应生成了乙烯 | |
| C. | 装置③可以证明苯生成溴苯的反应是取代反应 | |
| D. | 装置④可用于实验室制备硝基苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
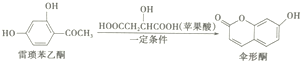
| A. | 雷梭苯乙酮有两种含氧官能团 | |
| B. | 1mol伞形酮与足量NaOH溶液反应,最多可消耗2mol NaOH | |
| C. | 伞形酮难溶于水 | |
| D. | 雷梭苯乙酮和伞形酮都能跟FeCl3溶液发生显色反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

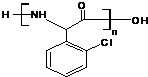 ;D→E所需X物质的结构简式:
;D→E所需X物质的结构简式:
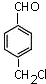 .
.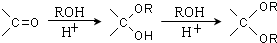
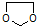 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:
的合成路线流程图(无机试剂任选).合成路线流程图示例如下:
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
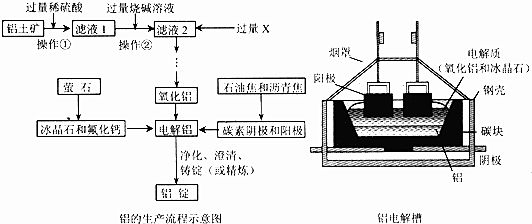
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 金属(粉末状)mol | 酸的浓度及体积 | 反应温度 | |
| A | Zn 0.1 | 6mol/L硝酸 10mL | 70℃ |
| B | Zn 0.1 | 3mol/L硫酸 10mL | 70℃ |
| C | Fe 0.1 | 3mol/L盐酸 10mL | 60℃ |
| D | Zn 0.1 | 3mol/L盐酸 10mL | 60℃ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com