
 4NO+6H2O
4NO+6H2O 4NO+6H2O
4NO+6H2O +HNO3(浓)
+HNO3(浓)| H2SO4(浓) |
| 50-60℃ |
 -NO2+H2O
-NO2+H2O +HNO3(浓)
+HNO3(浓)| H2SO4(浓) |
| 50-60℃ |
 -NO2+H2O
-NO2+H2O 4NO+6H2O,将苯滴入浓硝酸和浓硫酸混合液中,并在50℃--60℃反应的化学方程式为:
4NO+6H2O,将苯滴入浓硝酸和浓硫酸混合液中,并在50℃--60℃反应的化学方程式为: +HNO3(浓)
+HNO3(浓)| H2SO4(浓) |
| 50-60℃ |
 -NO2+H2O,
-NO2+H2O, 4NO+6H2O;
4NO+6H2O; +HNO3(浓)
+HNO3(浓)| H2SO4(浓) |
| 50-60℃ |
 -NO2+H2O;
-NO2+H2O;

科目:高中化学 来源: 题型:

| ||
| △ |
| ||
| △ |
查看答案和解析>>
科目:高中化学 来源:2011-2012学年浙江省宁波市高一下学期期末考试化学试卷(带解析) 题型:填空题
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:
(1)如图1是1 mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图(图中涉及物质均为气态),请写出NO2和CO反应的热化学方程式 。
(2)在0.5L的密闭容器中,充入一定量的氮气和氢气进行反应,三种气体的物质的量随时间的变化曲线如图2所示。则Y是 ,2min内N2的反应速率υ(N2)= 。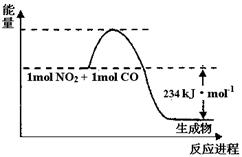
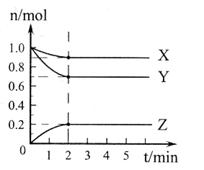
图1 图2
(3)硝酸工业在国民经济、国防工业和航天事业中占有重要地位。随着化学纤维、近代有机合成、火箭、导弹等工业的迅速发展,需要使用大量的硝酸。
①工业生产中用铂系金属作为催化剂,用氨氧化法制取硝酸。第一步反应为氨在催化剂作用下与氧气发生反应生成NO,写出反应化学方程式 。
②铜既能与稀硝酸反应,也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将方程式表示为:Cu+HNO3 →Cu(NO3)2+NO↑+NO2↑+H2O (方程式未配平)。反应中还原产物是 ,0.6mol Cu被硝酸完全溶解后,如果得到的NO和NO2物质的量相同,则得到标准状况下气体体积为 L。
查看答案和解析>>
科目:高中化学 来源:2010~2011学年浙江省台州市高一下学期期末考试化学 题型:填空题
(10分)硝酸工业在国民经济、国防工业和航天事业中占有重要地位。随着化学纤维、近代有机合成、火箭、导弹等工业的迅速发展,需要使用大量的硝酸。
(1)工业生产中用铂系金属作为催化剂,用氨氧化法制取硝酸。写出用铂铑合金作催化剂由氨氧化制备硝酸的第一步反应的化学方程式 ▲ 。浓硝酸和浓硫酸的混合酸是有机合成中常用的硝化剂,写出将苯滴入浓硝酸和浓硫酸混合液中,并在50℃--60℃反应的化学方程式 ▲ 。
(2)铜既能与稀硝酸反应,也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将方程式表示为:Cu+HNO3 → Cu(NO3)2+NO↑+NO2↑+H2O (方程式未配平)。则硝酸在该反应中的作用是 ▲ 。如果得到的NO和NO2物质的量相同,写出并配平该反应的离子方程式 ▲ ,0.6mol Cu被硝酸完全溶解后,若用排水法收集这些气体,可得标准状况下的气体体积为 ▲ 。
查看答案和解析>>
科目:高中化学 来源:2014届浙江省宁波市高一下学期期末考试化学试卷(解析版) 题型:填空题
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:
(1)如图1是1 mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图(图中涉及物质均为气态),请写出NO2和CO反应的热化学方程式 。
(2)在0.5L的密闭容器中,充入一定量的氮气和氢气进行反应,三种气体的物质的量随时间的变化曲线如图2所示。则Y是 ,2min内N2的反应速率υ(N2)= 。


图1 图2
(3)硝酸工业在国民经济、国防工业和航天事业中占有重要地位。随着化学纤维、近代有机合成、火箭、导弹等工业的迅速发展,需要使用大量的硝酸。
①工业生产中用铂系金属作为催化剂,用氨氧化法制取硝酸。第一步反应为氨在催化剂作用下与氧气发生反应生成NO,写出反应化学方程式 。
②铜既能与稀硝酸反应,也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将方程式表示为:Cu+HNO3 → Cu(NO3)2+NO↑+NO2↑+H2O (方程式未配平)。反应中还原产物是 ,0.6mol Cu被硝酸完全溶解后,如果得到的NO和NO2物质的量相同,则得到标准状况下气体体积为 L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com