
同温同压下,等质量的SO2和CO2相比较,下列叙述中正确的是()
A. 密度比为16:11 B. 密度比为11:16
C. 体积比为16:11 D. 原子数比为1:1
考点: 阿伏加德罗定律及推论.
分析: 同温同压下,气体摩尔体积相等,根据n=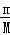 、ρ=
、ρ= 、V=nVm=
、V=nVm=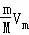 、N=
、N= 及分子构成分析解答.
及分子构成分析解答.
解答: 解:同温同压下,气体摩尔体积相等,根据ρ= 知,二者的密度之比等于其摩尔质量之比=64g/mol:44g/mol=16::1,故A正确;
知,二者的密度之比等于其摩尔质量之比=64g/mol:44g/mol=16::1,故A正确;
B.根据A知,二者的密度之比为16:11,故B错误;
C.根据V=nVm= 知,相同质量时,二者的体积之比等于摩尔质量的反比=44g/mol:64g/mol=11:16,故C错误;
知,相同质量时,二者的体积之比等于摩尔质量的反比=44g/mol:64g/mol=11:16,故C错误;
D.根据N= 及分子构成知,相同质量时,二者的原子个数之比与其摩尔质量成反比=44g/mol:64g/mol=11:16,故D错误;
及分子构成知,相同质量时,二者的原子个数之比与其摩尔质量成反比=44g/mol:64g/mol=11:16,故D错误;
故选A.
点评: 本题考查阿伏伽德罗定律及其推论,熟悉物质的量公式中各个物理量的关系是解本题关键,侧重考查学生对基本公式的灵活运用,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列关于过氧化钠的叙述正确的是()
A. 过氧化钠能与酸反应生成盐和水,所以过氧化钠是碱性氧化物
B. 可用Na2O2除去N2中的水蒸气
C. 过氧化钠与水反应时,过氧化钠是氧化剂,水是还原剂
D. 过氧化钠与二氧化碳反应时,过氧化钠既是氧化剂又是还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
某工厂的废渣中混有少量的锌粉和氧化铜(其他成分不跟酸反应),跟大量废盐酸接触形成污水,产生公害.若向污水中撒入铁粉且反应后铁粉有剩余,此时污水中一定含有的金属离子是( )
|
| A. | Fe2+、Cu2+ | B. | Cu2+、H+ | C. | Zn2+、Fe2+ | D. | Zn2+、H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)现有以下物质①NaCl溶液 ②干冰(固态的二氧化碳) ③醋酸 ④铜 ⑤BaSO4固体 ⑥蔗糖 ⑦酒精 ⑧熔融的KNO3,其中属于电解质的是 ;属于非电解质的是 ;能导电的是 .
(2)鲜榨苹果汁是人们喜爱的饮料.由于此饮料中含有Fe2+,现榨的苹果汁在空气中会由淡绿色的Fe2+变为棕黄色的Fe3+,这个变色的过程中的Fe2+被 (填“氧化”或“还原”).若在榨汁的时候加入适量的维生素C,可有效防止这种现象的发生,这说明维生素C具有 .
A、氧化性 B、碱性 C、酸性 D、还原性.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作正确的是()
A. 硫酸钠中含有少量碳酸钠,加入盐酸除去碳酸钠杂质
B. 萃取时,将酒精和碘化钾溶液放入分液漏斗中静置分层
C. 用分液漏斗分离互不相容的两种液体时,先放出下层液体,然后再放出上层液体
D. 配制一定物质的量浓度溶液定容时,用胶头滴管滴加蒸馏水至溶液凹液面最低点与刻度线相切
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室中需要配制2mol/L的NaCl溶液950mL,配制时应选用的容量瓶的规格和称取NaCl质量分别是()
A. 950mL,111.2g B. 500mL,117g
C. 1000mL,117g D. 1000mL,111.2g
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有机物中,既能发生加成反应,又能发生酯化反应,还能被新制Cu(OH)2悬浊液氧化的物质是()
A. CH3=CH﹣CHO B. CH3CH2COOH
C. CH2=CH﹣COOCH3 D. CH2OH(CHOH)4CHO
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示,三个烧瓶中分别充满NO2气体并分别放置在盛有下列物质的烧杯中.在(1)中加入无水CaCl2,在(3)中加入NH4Cl晶体,(2)中不加任何物质,发现(1)中NO2红棕色变深,(3)中NO2红棕色变浅,下列叙述不正确的是()
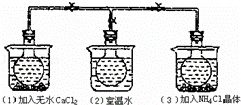
A. CaCl2溶于水时放出热量 B. 烧瓶(1)中气体的压强增大
C. NH4Cl溶于水时放出热量 D. 烧瓶(3)中气体的压强减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com