
ЎѕМвДїЎї°ґТЄЗуРґИИ»ЇС§·ЅіМКЅЈє
(1)ТСЦЄПЎИЬТєЦРЈ¬1 mol H2SO4УлNaOHИЬТєЗЎєГНкИ«·ґУ¦К±Ј¬·Еіц114.6 kJИИБїЈ¬Рґіц±нКѕH2SO4УлNaOH·ґУ¦µДЦРєНИИµДИИ»ЇС§·ЅіМКЅ______________________________Ј»
(2)25ЎжЎў101 kPaМхјюПВід·ЦИјЙХТ»¶ЁБїµД¶ЎНйЖшМе·ЕіцИИБїОЄQkJЈ¬ѕІв¶ЁЈ¬Ѕ«ЙъіЙµДCO2НЁИлЧгБїіОЗеКЇ»ТЛ®ЦРІъЙъ25 g°ЧЙ«іБµнЈ¬Рґіц±нКѕ¶ЎНйИјЙХИИµДИИ»ЇС§·ЅіМКЅ_________________________ЎЈ
Ўѕґр°ёЎї![]() H2SO4(aq)Ј«NaOH(aq)=
H2SO4(aq)Ј«NaOH(aq)=![]() Na2SO4(aq)Ј«H2O(l) ЎчH= -57.3kJ/mol C4H10ЈЁgЈ©+
Na2SO4(aq)Ј«H2O(l) ЎчH= -57.3kJ/mol C4H10ЈЁgЈ©+![]() O2ЈЁgЈ©=4CO2ЈЁgЈ©+5H2OЈЁlЈ© ЎчH=-16QkJЎ¤molЈ1
O2ЈЁgЈ©=4CO2ЈЁgЈ©+5H2OЈЁlЈ© ЎчH=-16QkJЎ¤molЈ1
ЎѕЅвОцЎї
ЈЁ1Ј©ФЪПЎИЬТєЦРЈ¬Лбёъјо·ўЙъЦРєН·ґУ¦ЙъіЙ1molЛ®К±µД·ґУ¦ИИЅРЧцЦРєНИИЈ»1molH2SO4УлNaOH·ґУ¦ЙъіЙ2molH2OЈ¬·Еіц114.6kJµДИИБїЈ¬ФтЙъіЙ1molH2O·Еіц57.3kJµДИИБїЈ¬±нКѕH2SO4УлNaOH·ґУ¦µДЦРєНИИµДИИ»ЇС§·ЅіМКЅОЄ![]() H2SO4(aq)Ј«NaOH(aq)=
H2SO4(aq)Ј«NaOH(aq)=![]() Na2SO4(aq)Ј«H2O(l) ЎчH=-57.3kJ/molЈ»
Na2SO4(aq)Ј«H2O(l) ЎчH=-57.3kJ/molЈ»
ЈЁ2Ј©25 g°ЧЙ«іБµнCaCO3ОпЦКµДБїОЄ25gЎВ100g/mol=0.25molЈ¬ёщѕЭCКШєгЈ¬C4H10ИјЙХЙъіЙБЛ0.25molCO2Ј¬Фт¶ЎНйОпЦКµДБїОЄ![]() Ј¬1molC4H10·ЕіцµДИИБїКЗQkJЎВ
Ј¬1molC4H10·ЕіцµДИИБїКЗQkJЎВ![]() =16QkJЈ¬±нКѕ¶ЎНйИјЙХИИµДИИ»ЇС§·ЅіМКЅОЄC4H10ЈЁgЈ©+
=16QkJЈ¬±нКѕ¶ЎНйИјЙХИИµДИИ»ЇС§·ЅіМКЅОЄC4H10ЈЁgЈ©+![]() O2ЈЁgЈ©=4CO2ЈЁgЈ©+5H2OЈЁlЈ© ЎчH=-16QkJЎ¤molЈ1ЎЈ
O2ЈЁgЈ©=4CO2ЈЁgЈ©+5H2OЈЁlЈ© ЎчH=-16QkJЎ¤molЈ1ЎЈ



| Дкј¶ | ёЯЦРїОіМ | Дкј¶ | іхЦРїОіМ |
| ёЯТ» | ёЯТ»Гв·СїОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СїОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СїОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СїОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СїОіМНЖјцЈЎ | іхИэ | іхИэГв·СїОіМНЖјцЈЎ |
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїПВБРИИ»ЇС§·ЅіМКЅЦРЈ¬ХэИ·µДКЗЈЁ Ј©
A. јЧНйµДИјЙХИИЎчH=©Ѓ890.3kJ/molЈ¬ФтјЧНйИјЙХµДИИ»ЇС§·ЅіМКЅїЙ±нКѕОЄЈєCH4ЈЁgЈ©+2O2ЈЁgЈ©ЁTCO2ЈЁgЈ©+2H2OЈЁgЈ©ЎчH=©Ѓ890.3kJ/mol
B. Т»¶ЁМхјюПВЈ¬Ѕ«0.5 molN2єН1.5molH2ЦГУЪГЬ±ХИЭЖчЦРід·Ц·ґУ¦ЙъіЙNH3·ЕИИ19.3kJЈ¬ЖдИИ»ЇС§·ЅіМКЅОЄЈєN2ЈЁgЈ©+3H2ЈЁgЈ©![]() 2NH3ЈЁgЈ©ЎчH=©Ѓ38.6kJ/mol
2NH3ЈЁgЈ©ЎчH=©Ѓ38.6kJ/mol
C. ТСЦЄ2C(s)Ј«2O2(g) ЁT2CO2(g)Ј»ЎчH1Ј»2C(s)Ј«O2(g)=2CO(g) ЎчH2 ФтЎчH1ЈѕЎчH2
D. ФЪ101kPaК±Ј¬2gH2НкИ«ИјЙХЙъіЙТєМ¬Л®Ј¬·Еіц285.8kJИИБїЈ¬ЗвЖшИјЙХµДИИ»ЇС§·ЅіМКЅ±нКѕОЄЈє2H2ЈЁgЈ©+O2ЈЁgЈ©ЁT2H2OЈЁlЈ©ЎчH=©Ѓ571.6kJ/mol
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїМъКЗИЛАаЙъ»оЦРЧоіЈјыЎўУ¦УГЧо№г·єµДЅрКфЈ¬ёЦМъФЪїХЖшЦРєЬИЭТЧ±»ёЇКґЎЈ
(1)іґ№эІЛµДМъ№шОґј°К±Пґѕ»ЈЁІРТєЦРє¬УР NaClЈ©Ј¬І»ѕГ±г»бТтёЇКґ¶шіцПЦєЦЙ«Рв°ЯЎЈМъ№шРвКґµДµзј«·ґУ¦КЅОЄЈєёєј«___________________________Ј¬Хэј«___________________________ЎЈ
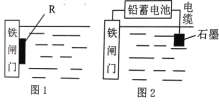
(2)ОЄБЛЅµµНДіЛ®ївµДМъХўГЕµДёЇКґЛЩВКЈ¬їЙТФІЙУГНј 1 ЛщКѕµД·Ѕ°ёЈ¬ЖдЦРєёЅУФЪМъХўГЕЙПµД№ММеІДБП R їЙТФІЙУГ _______________ ЈЁМоРтєЕЈ©ЎЈ
AЎўН BЎўРї CЎўДЖ DЎўКЇД«
(3)Нј 2 ЛщКѕµД·Ѕ°ёТІїЙТФЅµµНМъХўГЕµДёЇКґЛЩВКЈ¬ЖдЦРМъХўГЕУ¦ёГБ¬ЅУФЪЗ¦РоµзіШµД_______ј«ЙПЈЁМоЎ°ХэЎ±»тЎ°ёєЎ±Ј©ЎЈ
(4)іЈОВПВТФЗ¦РоµзіШОЄµзФґЈ¬УГКЇД«Ччµзј«µзЅв 1L 0.1mol/L NaClИЬТєЈ¬µзЅвТ»¶ОК±јдєуЈ¬ІвµГИЬТєµД pH ОЄ 13Ј¬ФтЗ¦РоµзіШЦРЧЄТЖµзЧУµДОпЦКµДБїОЄ__________ ЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїПВБРУР№Ш·ґУ¦ИИµДРрКцХэИ·µДКЗ
A.ТСЦЄ![]()
![]()
![]() Ј¬ФтЗвЖшµДИјЙХИИОЄ
Ј¬ФтЗвЖшµДИјЙХИИОЄ![]()
B.![]() Ј¬КЇД«
Ј¬КЇД«![]() Ј¬ЅрёХКЇ
Ј¬ЅрёХКЇ![]() Ј¬ЛµГчКЇД«±ИЅрёХКЇОИ¶Ё
Ј¬ЛµГчКЇД«±ИЅрёХКЇОИ¶Ё
C.![]() Ј¬
Ј¬![]() єгОВєгИЭМхјюПВґпµЅЖЅєвєујУИлXЈ¬ЙПКц·ґУ¦µД
єгОВєгИЭМхјюПВґпµЅЖЅєвєујУИлXЈ¬ЙПКц·ґУ¦µД![]() Фцґу
Фцґу
D.ТСЦЄ![]() Ј»
Ј»![]() Фт
Фт![]()
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїТТ°·ЈЁCH3ЈCH2ЈNH2Ј©ј«ТЧ»У·ўЈ¬ИЬУЪЛ®ЎўТТґјЎўТТГСµИЈ¬їЙУГУЪЙъІъИѕБПЎўТЅТ©єНАлЧУЅ»»»КчЦ¬µИЎЈЅ«ТТґјУл°±ЖшЦГУЪОВ¶ИОЄ350Ў«400ЎжЎўС№ЗїОЄ2.45Ў«2.94MPaєНґЯ»ЇјБОЄСх»ЇВБµДМхјюПВ·ґУ¦їЙЦЖ±ёТТ°·ЎЈ

ўсЈ®°±ЖшµДЦЖ±ё
ЈЁ1Ј©УГИзНјЛщКѕЧ°ЦГЦЖ±ёNH3ЎЈ
ўЩТЗЖчAµДГыіЖКЗ___ЎЈ
ўЪКФјБXїЙДЬКЗCaO»т__ЈЁМоКФјБГыіЖЈ©Ј¬ИфСЎФсCaOК±Ј¬ДЬІъЙъNH3µДФТтКЗ___ЎЈ
ўтЈ®ТТ°·µДЦЖ±ёУлМбґї
ЈЁ2Ј©ТТ°·µДЦЖ±ёЈє
ЙъіЙТТ°·ЈЁCH3CH2ЈNH2Ј©µД»ЇС§·ЅіМКЅОЄ___ЎЈЈЁїЙІ»Рґ·ґУ¦МхјюЈ©
ЈЁ3Ј©ТСЦЄЈєЦЖ±ё№эіМЦРіэБЛЙъіЙТТ°·НвЈ¬»№»бІъЙъ¶юТТ°·ЎўИэТТ°·ЎўТТГСЎўТТЗиєНТТП©ЎЈ

УГИзНјЧ°ЦГМбґїТТ°·Јє

ўЩМбґїТТ°·Ч°ЦГЦРµДТ»ґ¦ґнОуКЗ___ЎЈ
ўЪАдДэ№ЬµДАдЛ®ЈЁ10ЎжЈ©УЙ___ЈЁМоЎ°MЎ±»тЎ°NЎ±Ј©їЪБчіцЎЈ
ўЫґнОуѕАХэєуХфБуЈ¬КХјЇ___ЎжЧуУТµДБу·ЦЎЈ
ўЬ±щЛ®ФЎµДЧчУГКЗ___ЎЈ
ЈЁ4Ј©ТТґјµДГЬ¶ИОЄ0.8gЎ¤cmЈ3Ј¬ИфИЎ230.00mLОЮЛ®ТТґјЈ¬Ул№эБї°±Жш·ґУ¦єуЈ¬ѕМбґїєуµГµЅ142.02gТТ°·Ј¬ФтТТ°·µДІъВКОЄ__%ЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїЎ°СОЛ®¶ЇБ¦Ў±НжѕЯіµµДµзіШТФГѕЖ¬Ўў»оРФМїОЄµзј«Ј¬Птј«°еЙПµОјУКіСОЛ®єуµзіШ±гїЙ№¤ЧчЈ¬µзіШ·ґУ¦ОЄ2Mg+O2+2H2O = 2Mg (OH)2 ЎЈПВБР№ШУЪёГµзіШµДЛµ·ЁґнОуµДКЗ( )

A. КіСОЛ®ЧчОЄµзЅвЦКИЬТє
B. µзіШ№¤ЧчК±ГѕЖ¬ЧчОЄХэј«Ц𽥱»ПыєД
C. µзіШ№¤ЧчК±КµПЦБЛ»ЇС§ДЬПтµзДЬµДЧЄ»Ї
D. »оРФМїµзј«ЙПµД·ґУ¦ОЄO2+2H2O + 4eЈ = 4OH -
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїіЈОВПВЈ¬Ѕ«µИЕЁ¶ИµДNaOHИЬТє·Ц±рµОјУµЅµИpHЎўµИМе»эµДHAЈ¬HBБЅЦЦИхЛбИЬТєЦРЈ¬ИЬТєµДpHУлБЈЧУЕЁ¶И±ИЦµµД¶ФКэ№ШПµИзНјЛщКѕЎЈПВБРРрКцґнОуµДКЗ![]()
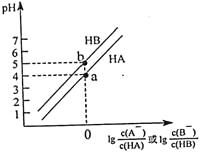
A.aЎўbБЅµгЈ¬ИЬТєЦРЛ®µДµзАліМ¶ИЈє![]()
B.µзАлЖЅєвіЈКэЈє![]()
C.aµгК±Ј¬![]()
D.ПтHAИЬТєЦРµОјУNaOHИЬТєЦБЦРРФК±Јє![]()
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎї¶ФУЪИЬТєµДЛбјоРФЛµ·ЁХэИ·µДКЗ
A.є¬OHЈµДИЬТєТ»¶ЁіКјоРФB.ФЪ100ЎгCК±Ј¬ґїЛ®µДpHЈј7Ј¬ТтґЛПФЛбРФ
C.c(H+)=c(OH-)µДИЬТєТ»¶ЁіКЦРРФD.pHЈЅ14µДИЬТєјоРФЧоЗї
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎї25ЎжК±Ј¬Л®ИЬТєЦРc(H+)Улc(OHЈ)µД±д»Ї№ШПµИзНјЦРЗъПЯa cЛщКѕЈ¬ПВБРЕР¶ПґнОуµДКЗ

A.a cЗъПЯЙПµДИОТвТ»µг¶јУРc(H+)Ў¤c(OHЈ)ЈЅ10-14
B.b dПЯ¶ОЙПИОТвТ»µг¶ФУ¦µДИЬТє¶јіКЦРРФ
C.dµг¶ФУ¦ИЬТєµДОВ¶ИёЯУЪ25ЎжЈ¬pHЈј7
D.CH3COONaИЬТєІ»їЙДЬО»УЪcµг
Ійїґґр°ёєНЅвОц>>
°Щ¶ИЦВРЕ - Б·П°ІбБР±н - КФМвБР±н
єю±±КЎ»ҐБЄНшОҐ·ЁєНІ»БјРЕПўѕЩ±ЁЖЅМЁ | НшЙПУРє¦РЕПўѕЩ±ЁЧЁЗш | µзРЕХ©ЖѕЩ±ЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРє¦РЕПўѕЩ±ЁЧЁЗш | ЙжЖуЗЦИЁѕЩ±ЁЧЁЗш
ОҐ·ЁєНІ»БјРЕПўѕЩ±Ёµз»°Јє027-86699610 ѕЩ±ЁУКПдЈє58377363@163.com