
| A�� | ���ݷ�ӦCu+H2SO4$\frac{\underline{\;���\;}}{\;}$CuSO4+H2�����Ƴ�Cu�Ļ�ԭ�Ա�H2��ǿ | |
| B�� | ��Cl2��������ǿ��I2�������ԣ������û���ӦI2+2NaClO3�T2NaIO3+Cl2���ܷ��� | |
| C�� | �������ữ��H2O2��Һ����Fe��NO3��2��Һ�У���Һ���ɫ��֤�������ԣ�H2O2��Fe3+ǿ | |
| D�� | ��2Na+2C+2NH3=2NaCN+3H2����Ӧ�еĻ�ԭ��ΪC��Na |
���� A�����ݸ÷�Ӧ�ڵ�������·����ģ������Է���������ԭ��Ӧ������
B������I2+2NaClO3�T2NaIO3+Cl2�ܷ�����˵���ⵥ�ʵĻ�ԭ��ǿ��������
C���������ữ�����������������ӡ���������ӷ���������ԭ��Ӧ��
D�����ݷ�Ӧǰ�ϼ�����Ϊ��ԭ���жϣ�
��� �⣺A����Ϊ�÷�Ӧ�ڵ�������·����ģ������Է���������ԭ��Ӧ�����Բ����Ƴ�Cu�Ļ�ԭ�Ա�H2��ǿ����A����
B��I2+2NaClO3�T2NaIO3+Cl2�ܷ�����˵���ⵥ�ʵĻ�ԭ��ǿ������������Cl2��������ǿ��I2�������ԣ���ⵥ�ʵĻ�ԭ��ǿ���������ʸ÷�Ӧ�ܷ�������B����
C���������ữ�����������������ӡ���������ӷ���������ԭ��Ӧ������˵�����������Ƿ���������ⷴӦ�����ܱȽ�H2O2��Fe3+�������ԣ���C����
D��2Na+2C+2NH3=2NaCN+3H2����Ӧ�У����ϼ۷�������ΪC��Na�����Ի�ԭ��ΪC��Na����D��ȷ��
��ѡD��
���� ���⿼��������ԭ��Ӧ�����Ի�ԭ�ԵıȽϣ����ط���������ԭ��Ӧ��ǿ�����ķ�Ӧԭ����ע�������Ӧ�ı��ʣ���Ŀ�ѶȲ���


 ����С��ʿ���������ϵ�д�
����С��ʿ���������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �о���ѧϰС�����CH4������̽��ʵ�飮
�о���ѧϰС�����CH4������̽��ʵ�飮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.01mol•L-1NH4Al��SO4��2��Һ��0.02mol•L-1Ba��OH��2��Һ�������ϣ�NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4��+Al��OH��3��+NH3•H2O | |
| B�� | һ�������£���0.5mol N2��g����1.5molH2��g�������ܱյ������г�ַ�Ӧ����NH3��g��������19.3kJ�����Ȼ�ѧ����ʽΪ��N2��g��+3H2��g��?2NH3��g����H=-38.6kJ•mol-1 | |
| C�� | ��ͼ��ʾH2��O2������Ӧ�����е������仯��H2��ȼ����Ϊ571.6 kJ•mol-1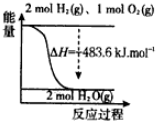 | |
| D�� | CO��g����ȼ������283.0 kJ•mol-1����CO2�ֽ���Ȼ�ѧ����ʽΪ��2CO2��g��=2CO��g��+O2��g����H=+283.0 kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����AgNO3��Һ | B�� | HCl��Һ | C�� | ϡNaOH��Һ | D�� | ����CuSO4��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 2-��-6-�һ�����
2-��-6-�һ����� 4��7��7-����-1-��ϩ
4��7��7-����-1-��ϩ�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����������Ի�ѧҩƷ���У��Ҵ�������������Һ�����Խ������������ﵽ������Ŀ�� | |
| B�� | ���������������ġ�PM2.5���Ƕ�һ���·��ӵ����� | |
| C�� | �ý��ݹ����������Һ�Ĺ���������ˮ�� | |
| D�� | ʩ��ʱ����ľ�ң���Ч�ɷ�ΪK2CO3����NH4Cl���ʹ��Ч������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | N2�� | B�� | NH3 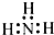 | C�� | H2O H+[��O��]2-H+ | D�� | NaCl  |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HI��HBr��HCl��HF | B�� | HCl��H2S��PH3��SiH4 | ||
| C�� | H2O��H2S��HCl��HBr | D�� | HF��H2O��PH3��NH3 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com