
| A£®K+”¢H+”¢SO42-”¢Al3+ | B£®Na+”¢Ca2+”¢CO32-”¢NO3- |
| C£®Na+”¢Fe3+”¢SCN-”¢SO42- | D£®Na+”¢H+”¢Cl-”¢HCO3- |
 ĒįĖÉæĪĢƵ„ŌŖĘŚÖŠĘŚÄ©×ØĢā³å“Ģ100·ÖĻµĮŠ“š°ø
ĒįĖÉæĪĢƵ„ŌŖĘŚÖŠĘŚÄ©×ØĢā³å“Ģ100·ÖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®OH£ | B£®Cl£ | C£®SO42£ | D£®NO3£ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗ¼ĘĖćĢā
 C6H6O6+2HI
C6H6O6+2HI ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ŌŚpH=1µÄČÜŅŗÖŠ£ŗNH4+”¢K+”¢ClO-”¢Cl- |
| B£®ÓŠSO42-“ęŌŚµÄČÜŅŗÖŠ£ŗNa+”¢Mg2+”¢Ba2+”¢I- |
| C£®ÓŠNO3-“ęŌŚµÄĒæĖįŠŌČÜŅŗÖŠ£ŗNH4+”¢Ba2+”¢Fe2+”¢Br- |
| D£®ŌŚc(H+)=1.0”Į10-13mol”¤L-1µÄČÜŅŗÖŠ£ŗNa+”¢K+”¢AlO2-”¢SO42- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Ģ¼ĖįøĘČÜÓŚ“×Ėį£ŗCaCO3+2H+=Ca2++H2O+CO2”ü |
| B£®ĻņNaHCO3ČÜŅŗÖŠµĪ¼ÓAlCl3ČÜŅŗ£ŗAl3£«+3HCO3£=Al(OH)3”ż + 3CO2”ü |
| C£®NH4HCO3ČÜÓŚ¹żĮæµÄNaOHČÜŅŗÖŠ£ŗHCO3£+OH£= CO32£+H2O |
| D£®SO2ĘųĢåĶØČĖBa(NO3)2ČÜŅŗÖŠ£ŗSO2+H2O+Ba2+=BaSO3”ż+2H+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
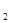 µÄČÜŅŗÖŠ£¬ĻĀĮŠø÷×éĄė×ÓŅ»¶Ø²»ÄÜ“óĮæ¹²“ęµÄŹĒ
µÄČÜŅŗÖŠ£¬ĻĀĮŠø÷×éĄė×ÓŅ»¶Ø²»ÄÜ“óĮæ¹²“ęµÄŹĒA£®Na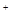 ”¢Fe ”¢Fe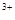 ”¢SO ”¢SO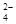 ”¢Cl ”¢Cl |
B£®Ba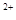 ”¢Mg ”¢Mg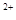 ”¢HCO ”¢HCO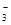 ”¢NO ”¢NO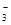 |
C£®Na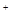 ”¢K ”¢K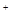 ”¢NO ”¢NO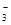 ”¢CO ”¢CO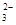 |
D£®K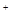 ”¢NO ”¢NO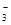 ”¢AlO ”¢AlO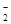 ”¢OH ”¢OH |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Na+”¢H+”¢NO3-”¢Cl- | B£®K+”¢H+”¢Cl-”¢SO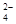 |
| C£®Ca2+”¢NO3-”¢HCO3-”¢Cl- | D£®Fe3+”¢NH4+”¢SCN-”¢Cl- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®H£«”¢K£«”¢HCO3”Ŗ”¢Ca2£« | B£®OH£”¢Na£«”¢Mg2£«”¢HCO3”Ŗ |
| C£®Na£«”¢SiO32”Ŗ”¢H£«”¢Cl£ | D£®K£«”¢H£«”¢Cl£”¢NO3”Ŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ÄÜŹ¹·ÓĢŖ±äŗģµÄČÜŅŗÖŠ£ŗAlO2£”¢Na+”¢NH4+”¢NO3£ |
| B£®25”ę,ÓÉĖ®µēĄė³öµÄc(H+)=1”Į10-12 mol”¤L-1µÄČÜŅŗÖŠ£ŗK+”¢Na+”¢SO42£ HCO3£ |
| C£®³£ĪĀĻĀ£¬ŌŚc£ØH+£©/c£ØOH-£©=1”Į10-12µÄČÜŅŗÖŠ£ŗNa+”¢CO32£”¢Cl£”¢NO3£ |
| D£®ŌŚĖįŠŌKMnO4ČÜŅŗÖŠ£ŗNa+”¢I£”¢SO42£”¢NO3£ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com