
| A、1 mol 氯气与足量氢氧化钠溶液完全反应,转移电子数目为2NA |
| B、14g氮气中含有14 NA个原子 |
| C、1L1.00 mol/L的Na2SO4溶液中Na+离子数目为2NA |
| D、11.2 L氢气中含有NA个氢原子 |
| m |
| M |


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:
| A、钢铁腐蚀时负极发生的反应:Fe→Fe 3++3e- | ||
| B、明矾水解的离子方程式:Al3++3H2O?Al(OH)3(胶体)+3H+ | ||
C、小苏打在水中的电离方程式:NaHCO3=Na++H++C
| ||
| D、1 g氢气在空气中完全燃烧生成液态水时放出285.8 kJ热量,其热化学方程式为:2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 阳离子 | H+、Na+、Al3+、Ag+、Ba2+ | ||||||
| 阴离子 | OH-、Cl-、C
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| A、将2.4 g碳完全转化为水煤气,然后再燃烧,整个过程△H=-78.7 kJ/mol?? |
| B、H的燃烧热为241.8 kJ/mol?? |
| C、由反应②可推知,CO具有还原性而没有氧化性 |
| D、由反应③可知,反应过程中转移5 mol电子且生成液态水时放出的热量小于604.5 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、MnO-4>Fe3+>Cl2>I2 |
| B、Cl2>I2>Fe3+>MnO4 |
| C、MnO-4>Cl2>Fe3+>I2 |
| D、Fe3+>MnO-4>Cl2>I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
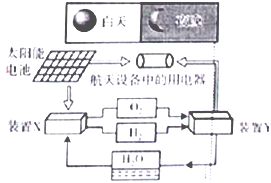 如图是一种航天器能量储存系统原理示意图.下列说法正确的是
如图是一种航天器能量储存系统原理示意图.下列说法正确的是| A、该系统中只存在3种形式的能量转化 |
| B、装置Y中负极的电极反应式为:O2+2H2O+4e-=4OH- |
| C、装置X能实现燃料电池的燃料和氧化剂再生 |
| D、该系统能实现物质的零排放,并能实现化学能与电能间的完全转化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )| A、5.4g水中含氢原子数为0.3NA |
| B、25℃,1L pH=12的氨水中,含有OH-的数目为0.1 NA |
| C、标准状况下,32g硫(结构如图)含S-S的数目为NA |
| D、在反应KIO3+6HI=3I2+KI+3H2O中,每生成l mol I2转移电子数为2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 电子转移 | 反应的Al | 溶液中的AlO2- | 生成的H2 | |
| A | 0.2NA | 0.1NA | ||
| B | 0.3NA | 0.3NA | ||
| C | 2.7g | 3.36L | ||
| D | 0.1NA | 2.7g |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com