
淀粉溶液是一种胶体,并且淀粉遇到碘单质,可以出现明显的蓝色特征。现将淀粉和稀Na2SO4溶液混合,装在半透膜中,浸泡在盛蒸馏水的烧杯内,过一段时间后,取烧杯中液体进行实验,能证明半透膜完好无损的是 ( )
A.加入BaCl2溶液产生白色沉淀 B.加入碘水不变蓝
C.加入BaCl2溶液产生没有白色沉淀产生 D.加入碘水变蓝
科目:高中化学 来源:2015届浙江省高三上学期期中联考化学试卷(解析版) 题型:实验题
(共12分)
MnO2是一种重要的无机功能材料,粗MnO2的提纯是工业生产的重要环节。某研究性学习小组设计了将粗MnO2(含有较多的MnO和MnCO3)样品转化为纯MnO2实验,其流程如下:

(1)第①步加稀H2SO4时,粗MnO2样品中的 (写化学式)转化为可溶性物质。
(2)第②步反应的离子方程式是
□ + □ClO3— + □ = □MnO2↓ + □Cl2↑ + □ 。
(3)第③步蒸发操作必需的仪器有铁架台(含铁圈)、酒精灯、 、 。
已知蒸发得到的固体中含有NaClO3和NaOH,则一定还含有 (写化学式)。
(4)用浓硫酸来配制本实验需要的稀硫酸,进行如下操作,其中会使所配溶液浓度偏高的是
A用量筒量取浓硫酸倒入小烧杯后,用蒸馏水洗涤量筒并将洗涤液转移到小烧杯中
B定容时仰视
C用量筒量取浓硫酸时,读数时仰视
D容量瓶中有水,未进行干燥
(5)若粗MnO2样品的质量为12.69g,第①步反应后,经过滤得到8.7g MnO2,并收集到0.224L CO2(标准状况下),则在第②步反应中至少需要 mol NaClO3。
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高三10月月考化学试卷(解析版) 题型:选择题
某一有机物A可发生如下反应:已知C为羧酸,且C、E均不发生银镜反应,则A的可能结构有

A.1种 B.2种
C.3种 D.4种
查看答案和解析>>
科目:高中化学 来源:2015届河南郑州市高三上第一次(10月)月考化学试卷(解析版) 题型:选择题
Na2FeO4是一高效多功能水处理剂,应用前景广阔。一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2 = 2Na2FeO4+2Na2O+2Na2SO4+O2↑。对此反应下列说法中正确的是( )
A.Na2O2在反应中只作氧化剂
B.Na2FeO4既是氧化产物又是还原产物
C.O2是还原产物
D.2 mol FeSO4发生反应时,反应中共有8摩尔电子发生转移
查看答案和解析>>
科目:高中化学 来源:2015届河南郑州市高三上第一次(10月)月考化学试卷(解析版) 题型:选择题
把足量的铁粉投入到稀盐酸和氯化铜的混合溶液中,充分反应后,残余固体的质量与原来加入 的铁粉质量相等,则原溶液中H+ 和Cl-的物质的量之比为( )
A.1∶4 B.1∶7 C.1∶8 D.2∶5
查看答案和解析>>
科目:高中化学 来源:2015届河南省10月联考化学试卷(解析版) 题型:实验题
(9分)超氧化钾(KO2)又称为化学氧自救剂,容易与空气中的水、二氧化碳等发生反应,主要用于煤矿井下急救。某兴趣小组拟选用如下装置制备超氧化钾(部分夹持仪器已略去)。
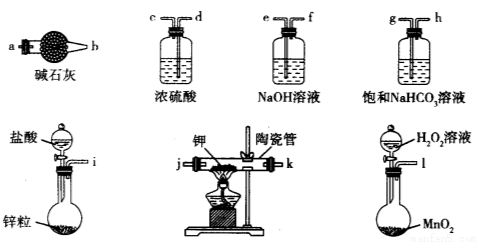
请回答下列问题:
(1)请选择必要的装置,按气流方向的连接顺序为____________________(填仪器接口的字母)。
(2)请根据完整的实验装置,完成下列实验步骤:①_____________________;②装入药品,打开分液漏斗活塞;③持续通入气体一段时间后,点燃酒精灯进行反应;④反应结束后,熄灭酒精灯,待反应管冷却至室温,停止通入氧气,并关闭分液漏斗的活塞;⑤拆除装置,取出产物。
(3)数据记录如下:

根据数据计算可得实验式KOx,则x=____________________。
(4)超氧化钾可吸收二氧化碳,并生成氧气,因此可以作为飞船、潜艇等密闭系统的氧气再生剂。写出超氧化钾与二氧化碳反应的化学方程式:____________________________________。与过氧化钠相比,其优点是____________________________________。
查看答案和解析>>
科目:高中化学 来源:2015届河南省10月联考化学试卷(解析版) 题型:选择题
某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Al3+和K+。取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;过虑,洗涤,灼烧,得到1.6g固体;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀。由此可知原溶液中( )
A.至少存在5种离子 B. Cl--一定存在,且c(Cl‑)≥0.4mol/L
C.SO42-、NH4+一定存在,Cl-可能不存在 D.CO32-、Al3+一定不存在,K+可能存在
查看答案和解析>>
科目:高中化学 来源:2015届河南省洛阳市高三上学期期中考试化学试卷(解析版) 题型:选择题
取一定量的铝土矿(含Al2O3、Fe2O3、SiO2)样品,放入盛有100mL H2SO4溶液的烧杯中,充分反应后过滤,向滤液中加入10mol·L-1的NaOH溶液,产生沉淀的质量与所加NaOH溶液的体积的关系如下图所示.则原H2SO4物质的量浓度是

A.1mol·L-1 B.2mol·L-1
C.3mol·L-1 D.4mol·L-1
查看答案和解析>>
科目:高中化学 来源:2014-2015学年陕西省高三上学期期中理综化学试卷(A)(解析版) 题型:填空题
[化学——选修3:物质结构与性质](15分)
汽车作为一种现代交通工具正在进入千家万户,汽车尾气的污染问题也成为当今社会急需解决的问题。为使汽车尾气达标排放,催化剂及载体的选择和改良是关键。目前我国研制的稀土催化剂催化转化汽车尾气示意图如图甲:
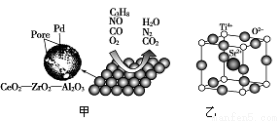
(1)下列有关说法正确的是________。
A.C3H8中碳原子都采用的是sp3杂化
B.O2、CO2、NH3都是非极性分子
C.每个N2中,含有2个π键
(2)CO的一种等电子体为NO+,NO+的电子式为
(3)CO与Ni可生成羰基镍[Ni(CO)4],已知其中镍为0价,镍原子在基态时,核外电子排布式为___________;[Ni(CO)4]的配体是________,配位原子是________。
(4)Zr原子序数为40,价电子排布式为4d25s2,它在周期表中的位置是________。
(5)为了节省贵重金属并降低成本,也常用钙钛矿型复合氧化物催化剂。一种复合氧化物晶体结构如图乙,则与每个Sr2+紧邻的O2-有________个。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com