
锗(Ge)、锡(Sn)、铅(Pb)与碳、硅两元素同位于第ⅣA族,其原子序数按锗、锡、铅的顺序依次增大,则下列推断一定不正确的是
A.锗、锡在空气中不反应,铅在空气中表面生成一层氧化铅
B.锗与盐酸不反应,锡、铅能与盐酸反应
C.锗、锡、铅的+4价氢氧化物的碱性:Ge(OH)4<Sn(OH)4<Pb(OH)4
D.锗、锡、铅的金属性依次减弱
【知识点】同一主族内元素性质递变规律与原子结构的关系 E2
【答案解析】D 解析:A、锗、锡、铅属于同主族元素,铅的原子序数大,则铅金属性强,锗、锡在空气中可能不反应,铅在空气中表面生成一层氧化铅,故A正确; B、锗与硅的单 质都能作半导体,化学性质相似,所以与盐酸不反应,锡、铅在金属活动顺序表中排在氢的前面,能与盐酸反应,故B正确; C、同主族从上到下金属性增强,所以
质都能作半导体,化学性质相似,所以与盐酸不反应,锡、铅在金属活动顺序表中排在氢的前面,能与盐酸反应,故B正确; C、同主族从上到下金属性增强,所以 锗、锡、铅的金属性依次增强,则其对应最高价氧化物的水化物的碱性依次增强,碱性:Ge(OH)4<Sn(OH)4<Pb(OH)4,故C正确; D、同主族从上到下金属性增强,所以锗、锡、铅的金属性依次增强,故D错误。
锗、锡、铅的金属性依次增强,则其对应最高价氧化物的水化物的碱性依次增强,碱性:Ge(OH)4<Sn(OH)4<Pb(OH)4,故C正确; D、同主族从上到下金属性增强,所以锗、锡、铅的金属性依次增强,故D错误。
【思路点拨】本题考查了同主族元素性质的递变规律,注意根据元素周期律分析,侧重金属元素的性质的考查,题目难度不大。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
某研究性学习小组欲测定室温下(25 ℃、101 kPa)的气体摩尔体积,请回答以下问题。
该小组设计的简易实验装置如图所示:
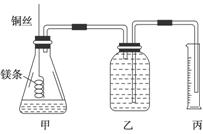
该实验的主要操作步骤如下:
①配制100 mL 1.0 mol·L-1的盐酸溶液;
②用________(填仪器名称并注明规格)量取7.5mL 1.0 mol·L-1的盐酸溶液加入锥形瓶中;
③称取a g已除去表面氧化膜的镁条,并系于铜丝末端,为使HCl全部参加反应,a的数值至少为________;
④往广口瓶中装入足量水,按上图连接好装置,检查装置的气密性;
⑤反应结束后待体系温度恢复到室温,读出量筒中水的体积为V mL。
请将上述步骤补充完整并回答下列问题。
(1)步骤①中,配制100 mL 1.0 mol·L-1的盐酸溶液时,下列哪些操作会使配制浓度偏小(填写字母) 。
A.用量筒量取浓盐酸时,俯视量筒的刻度
B.容量瓶未干燥即用来配制溶液
C.浓盐酸在烧杯中稀释时,搅拌时间过长
D.定容完成后,将容量瓶倒置摇匀后,发现液面低于刻度线
E.在容量瓶中定容时俯视容量瓶刻度线
F.烧杯中有少量水
(2)请填写操作步骤中的空格:步骤②_______________ 步骤③___________
(3)实验步骤⑤中应选用__________(填字母)的量筒。
A.100 mL B.200 mL C.500 mL
(4)读数时除恢复到室温外,还要注意
①______________________________,②_________________________________。
(5)忽略水蒸气影响,在该条件下测得气体摩尔体积的计算式为Vm=____L/mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子能够大量共存的是
A.无色溶液中:Fe3+、Na+、NO3-、Cl-
B.pH=0的溶液中:Fe2+、NO3-、Cl-、HCO3-
C.含MnO4-的溶液中:Fe3+、SO42-、NO3-、Mg2+
D.与铝作用生成氢气的溶液:Mg2+、NO3-、K+、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
下列图示与对应的叙述相符的是
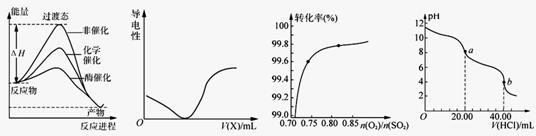
图1 图2 图3 图4
A.由图1所示曲线可知,化学催化比酶催化的效果好
B.在H2S溶液导电性实验中,由图2所示曲线可确定通入的气体X为Cl2
C.在其它条件不变时,2SO2(g)+ O2(g) 2SO3(g)转化关系(图3)中,纵坐标表示O2的转化率
2SO3(g)转化关系(图3)中,纵坐标表示O2的转化率
D.图4是用0.l000 mol·L-1的盐酸滴定20.00 mL 0.l000mol·L-1 Na2CO3溶液的曲线,从a→b点反应的离子方程式为:HCO3-+H+ = CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
亚硝酸(HNO2)是一种与醋酸酸性相当的弱酸,很不稳定,通常在室温下立即分解。
(1)在酸性条件下,当NaNO2与KI按物质的量1:1恰好完全反应,且I-被氧化为I2时,产物中含氮的物质为__________(填化学式)。
(2)要得到稳定的HNO2溶液,可以往冷冻的浓NaNO2溶液中加入或通入某种物质,下列物质不适合使用是_________(填序号)。
a.稀硫酸 b.二氧化碳 c.二氧化硫 d.磷酸
(3)工业废水中的NO2-可用铝粉除去.已知此反应体系中包含Al、NaAlO2、NaNO2、NaOH、NH3、H2O六种物质.将氧化剂和还原剂的化学式及其配平后的系数填入下列横线上:_________________________ + _________________________
上述反应后废水的pH值将________(填“增大”、“减小”或“不变”)。
(4)向20mL 0.01mol·L-1的NaNO2溶液中加入10mL 0.01 mol·L-1的AgNO3溶液,一段时间后,溶液中的c(Ag+)=________________________________。(已知:KSP(AgNO2)=2×10-8 mol2·L-2)
查看答案和解析>>
科目:高中化学 来源: 题型:
25℃时,将稀氨水逐滴滴加到稀硫酸中,当溶液的pH=7时,下列关系正确的是
A. c(NH4+)=c(SO42-) B. c(NH4+)>c(SO42-)
C. c(NH4+)<c(SO42-) D. c(NH4+)+c(SO42-)= c(H+)=c(NH4+)
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学科研小组研究合成氨:N2(g)+3H2(g)  2NH3(g);△H<0,在其他条件不变时,改变某一条件时对化学平衡的影响,得到如下图像,以下对应选项中正确的是( )
2NH3(g);△H<0,在其他条件不变时,改变某一条件时对化学平衡的影响,得到如下图像,以下对应选项中正确的是( )




A.(1)对应的是:在t1时恒压条件下,通入NH3
B. (2)对应的是:氨气在恒容不同温度下的百分含量
(2)对应的是:氨气在恒容不同温度下的百分含量
C.(3)对应的是:在恒容条件下,反应速率与温度的关系
D.(4)对应的是:N2转化率与温度(T1>T2)、压强的关系
查看答案和解析>>
科目:高中化学 来源: 题型:
有一固体混合物,可能由Na2CO3、Na2SO4、CuSO4、CaCl2、NaCl等物质组成。某同学为了鉴别它们,做了如下实验:
①将固体混合物溶于水,搅拌后得无色透明溶液;
②在①所得的溶液中滴加Ba(NO3)2溶液,有白色沉淀生成,并继续滴加至沉淀完全;
③过滤,然后在所得白色沉淀上加入过量稀硝酸,沉淀部分溶解。
根据该同学实验请你回答:
(1)原混合物中肯定有 ,肯定没有 ,可能含有 。
(2)写出上述实验过程中,可能发生反应的离子方程式:
。
(3)要检验可能含有的物质可采用的方法是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com