
| A. | R的氧化物都能溶于水 | |
| B. | R的最高价氧化物对应的水化物都是H2RO4 | |
| C. | R一定是非金属元素 | |
| D. | R的最高价氧化物都能与NaOH溶液反应 |
分析 R代表短周期元素,R原子最外层的p亚层上的未成对电子只有2个,则R的价层电子排布可能为2s22p2、2s22p4、3s23p2、3s23p4,可能为C、O、Si、S等元素,结合元素对应的单质、化合物的性质解答.
解答 解:R原子最外层的p亚层上的未成对电子只有2个,则R的价层电子排布可能为2s22p2、2s22p4、3s23p2、3s23p4,可能为C、O、Si、S等元素,则
A.如R为Si,对应的氧化物SiO2不能溶于水,故A错误;
B.如R为C、Si,则R的最高价氧化物所对应的水化物是H2SO3,故B错误;
C.R可能为C、O、Si、S等元素,一定是非金属元素,故C正确;
D.如R为C,对应的氧化物有CO,为不成盐氧化物,不能与NaOH溶液反应,故D错误.
故选C.
点评 本题考查原子结构与元素周期律的关系,为高频考点,侧重于学生的分析能力的考查,题目难度不大,本题注意把握常见元素的核外电子排布,根据核外电子排布特点正确判断元素的种类,把握常见元素化合物的性质.


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:解答题
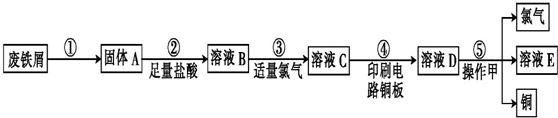
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲苯分子中的所有原子可能共平面 | |
| B. | CH2═CH-C6H5分子中的所有原子可能共平面 | |
| C. | 乙烷分子中的所有原子可能共平面 | |
| D. | 二氯甲烷分子为正四面体结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 温度℃ | 10 | 30 | 60 | 90 |
| 浓度(mol/L) | 0.21 | 0.17 | 0.14 | 0.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
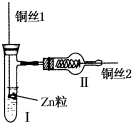 如图为氢气还原氧化铜的微型快速实验装置.实验前先将铜丝1处理成下端弯曲的小圆环,并用铁锤击成带小孔的小匙,将铜丝2一端弯曲成螺旋状.试回答下列问题:
如图为氢气还原氧化铜的微型快速实验装置.实验前先将铜丝1处理成下端弯曲的小圆环,并用铁锤击成带小孔的小匙,将铜丝2一端弯曲成螺旋状.试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
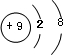 ,该元素与金属性最强的元素形成的化合物的电子式为
,该元素与金属性最强的元素形成的化合物的电子式为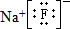 ;该化合物中存在的化学键为离子键 (选填“离子键”或“共价键”).
;该化合物中存在的化学键为离子键 (选填“离子键”或“共价键”).查看答案和解析>>
科目:高中化学 来源: 题型:推断题
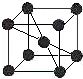 A、B、C、D、E五种元素均位于前四周期,原子序数逐渐增大,只有两种是金属元素.A、B、D三种元素在周期表中相对位置如图,其中A的价层电子排布为ns2np3,C的基态原子的第I电离能远小于第II电离能.E是第四期第IB族元素,回答下列问题:
A、B、C、D、E五种元素均位于前四周期,原子序数逐渐增大,只有两种是金属元素.A、B、D三种元素在周期表中相对位置如图,其中A的价层电子排布为ns2np3,C的基态原子的第I电离能远小于第II电离能.E是第四期第IB族元素,回答下列问题:| A | B | |
| D |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 若pH=7,HA的浓度一定为0.1 mol•L-1 | |
| B. | 若pH>7,HA的pH不可能等于1 | |
| C. | 若pH<7,溶液中的微粒浓度关系为:c(Na+)=c(HA)+c(A-) | |
| D. | 若pH=12,且HA为强酸时,HA的浓度应为0.08 mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com