
| A. | ①②③④⑤ | B. | ①③④⑤⑥ | C. | ①②③⑤⑥ | D. | 只有①②③ |
分析 根据反应AlCl3+3NaOH═Al(OH)3↓+3NaCl、Al(OH)3+NaOH═NaAlO2+2H2O,并利用a、b的大小来分析.
解答 解:若a:b=1:3时,发生AlCl3+3NaOH═Al(OH)3↓+3NaCl,生成沉淀的物质的量等于AlCl3的物质的量,即为amol,故①可能;
若a:b=1:3时,发生AlCl3+3NaOH═Al(OH)3↓+3NaCl,生成沉淀的物质的量等于AlCl3的物质的量,也等于bmol×$\frac{1}{3}$=$\frac{b}{3}$mol,故④可能;
若3:1≤b:a≤4:1时,发生AlCl3+3NaOH═Al(OH)3↓+3NaCl、Al(OH)3+NaOH═NaAlO2+2H2O,生成沉淀的物质的量等于amol-(b-3a)mol=(4a-b)mol,故⑥可能;
若3:1≤b:a≤4:1时,且b=3a+$\frac{2}{3}$a,发生AlCl3+3NaOH═Al(OH)3↓+3NaCl、Al(OH)3+NaOH═NaAlO2+2H2O,生成沉淀的物质的量等于amol-$\frac{2}{3}$amol=$\frac{a}{3}$mol,故③可能;
若b≥4a,发生AlCl3+4NaOH═NaAlO2+2H2O+3NaCl,则生成沉淀的物质的量为0,故⑤可能;
故选B.
点评 本题考查化学方程式有关计算,为高频考点,明确碱量的多少对化学反应的影响是解本题关键,注意利用极限和区间的方法来分析生成沉淀的几种可能性,题目难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.6g | B. | 0.32g | C. | 3.2g | D. | 6.4g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
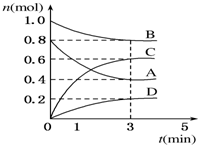 T℃时,在容积为0.5L的密闭容器中发生如 下反应.mA(g)+nB(g)?pC(g)+qD(s)△H<0(m、n、p、q为最简整数比).A、B、C、D的物质的量变化如图所示.
T℃时,在容积为0.5L的密闭容器中发生如 下反应.mA(g)+nB(g)?pC(g)+qD(s)△H<0(m、n、p、q为最简整数比).A、B、C、D的物质的量变化如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 溶液中只有气体产生 | |
| B. | 溶液中只有沉淀产生 | |
| C. | 溶液中有反应:Ca2++OH-+HCO-3═CaCO3↓+H2O发生 | |
| D. | 溶液中有反应:Ca2++2OH-+2HCO-3═CaCO3↓+CO32-+2H2O发生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷的标准燃烧热为-890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | 500℃、300 MPa下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)$?_{500℃、300MPa}^{催化剂}$ 2NH3(g)△H=-38.6kJ•mol-1 | |
| C. | 氯化镁溶液与氨水反应:Mg2++2OH-═Mg(OH)2↓ | |
| D. | 氧化铝溶于NaOH溶液:A12O3+2OH-═2AlO${\;}_{2}^{-}$+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
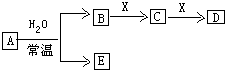 由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如图转化关系(部分生成物和反应条件略去).
由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如图转化关系(部分生成物和反应条件略去). ;
;查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com