



 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:高中化学 来源: 题型:
| A、制备Fe(OH)3胶体通常是将Fe(OH)3固体溶于沸水 |
| B、可利用过滤的方法区分溶液和胶体 |
| C、直径介于1nm~100nm之间的微粒称为胶体 |
| D、胶体介于溶液和浊液之间,在一定条件下能稳定存在,属于介稳体系 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度 | K1 | K2 |
| 973K | 1.47 | 2.38 |
| 1173K | 2.15 | 1.67 |
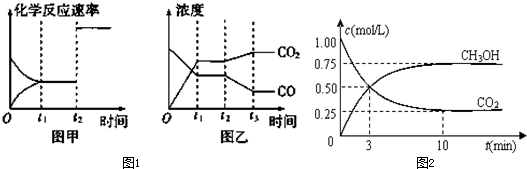
| ||
| 101kPa |
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知醋酸和盐酸是日常生活中极为常见的酸,在一定条件下,CH3COOH溶液中存在电离平衡:CH3COOH?CH3COO-+H+;△H>0
已知醋酸和盐酸是日常生活中极为常见的酸,在一定条件下,CH3COOH溶液中存在电离平衡:CH3COOH?CH3COO-+H+;△H>0| 测定次序 | 第一次 | 第二次 | 第三次 | 第四次 |
| V(mL) | 19.40 | 15.10 | 14.90 | 15.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用25mL的碱式滴定管量取14.80 mL KMnO4溶液 |
| B、实验时手指不小心沾上苯酚时,立即用70℃以上的热水清洗 |
| C、用广泛pH试纸测得某溶液的pH为3.5 |
| D、用25.00mL移液管移取稀盐酸25.00mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 现象或原理 |
| A | 取少量KI溶液,先滴加氯水,再加入少量苯,振荡、静置 | 溶液分层,下层呈紫红色 |
| B | 将稀盐酸或氢氧化钠溶液慢慢滴入氢氧化铝胶体中 | 均先沉淀后溶解 |
| C | 将浓硝酸加入盛有铂、金的烧杯中,不反应,加入一定量浓盐酸后,铂、金溶解 | 浓盐酸氧化性强于浓硝酸 |
| D | 将40.0g NaOH固体溶于1.0L蒸馏水中配成溶液 | 溶液物质的量浓度为1.0mol?L-1 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com