
һ���¶���,��2 L���ܱ�������,X��Y��Z�������������ʱ��仯��������ͼ��ʾ: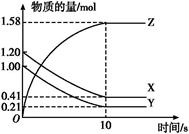
(1)�ӷ�Ӧ��ʼ��10 sʱ,��Z��ʾ�ķ�Ӧ����Ϊ����������������,X�����ʵ���Ũ�ȼ�������������,Y��ת����Ϊ������
(2)�÷�Ӧ�Ļ�ѧ����ʽΪ��
(3)10 s���ijһʱ��(t1)�ı����������,��������ʱ��ı仯ͼ����ͼ��ʾ: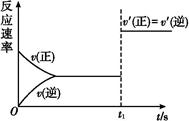
������˵�����ϸ�ͼ���������������
| A��t1ʱ��,������X��Ũ�� | B��t1ʱ��,��������ϵ�¶� |
| C��t1ʱ��,��С��������� | D��t1ʱ��,ʹ���˴��� |
 ����ѵ�����⿼ϵ�д�
����ѵ�����⿼ϵ�д� �������ϵ�д�
�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
298 Kʱ��ij�ݻ��̶�Ϊ1 L���ܱ������з������¿��淴Ӧ��A(g) 2B(g)����H��-a kJ��mol��1������B�����ʵ���Ũ����ʱ��仯��ͼ��ʾ��
2B(g)����H��-a kJ��mol��1������B�����ʵ���Ũ����ʱ��仯��ͼ��ʾ��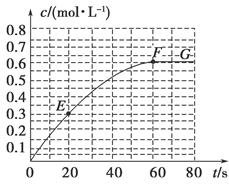
�Իش��������⡣
��1����֪298 Kʱ60 s�ﵽƽ�⣬�Ƚ�40��60 s�ں�60��80s��B��ƽ����Ӧ����:v(40��60) v(60��80)(�������������)��
��2����298 K�ﵽƽ��ʱ��B��ƽ��Ũ��ΪA��3�������ų�����x kJ����ʼ����A�����ʵ����� mol��
��3��298kʱ���÷�Ӧ��ƽ�ⳣ��Ϊ mol/L��
��4������Ӧ��298 K���У���1 L�ܱ������м���1 mol B��0.2 mol Ne���ﵽƽ��ʱ����������y kJ����ʱB��ת����Ϊ (�����)��
A������60% B������40%
C��С��40% D������40%��60%֮��
��5����ϣ�2������4��������ݣ�д��a��x��y���ߵĵ�ʽ��ϵʽ�� ��
��6������Ӧ��298K���У���Ӧ��ʼŨ��Ϊc(A)=c(B)=1.0mol/L����ѧƽ�⽫ (�����������)�ƶ���
��7����֪��������������֮�����ߵ�б�ʱ�ʾ��ʱ�����B��ƽ����Ӧ����(����ֱ��EF��б�ʱ�ʾ20 s��60 s��B��ƽ����Ӧ����)��������������һ�������б�ʵ������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��ӦA��3B=2C��2D�����ֲ�ͬ����µķ�Ӧ���ʿɷֱ�Ϊ
��v
| A����0.15 mol/(L��s)����v | B����0.6 mol/(L��s)����v | C����0.4 mol/(L��s)����v | D����0.45 mol/(L��s) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��һ�������£���������������������·�Ӧ��2SO2��g��+O2��g��?2SO3��g������H��0��
��1��д���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽK=
��2�������¶ȣ��÷�ӦKֵ ����������ת���� ����ѧ��Ӧ���� �����Ͼ�������С�䣩��
��3��600��ʱ����һ�ܱ������У������������������ϣ���Ӧ������SO2��O2��SO3���ʵ����仯��ͼ����Ӧ����ƽ��״̬��ʱ���� ��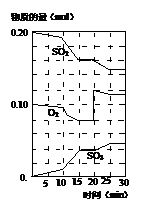
��4����ͼ�жϣ���Ӧ������20minʱ�����߷����仯��ԭ���� �������ֱ����
��5��10min��15min�����߱仯��ԭ������� ����д��ţ���
a�����˴��� b����С�������
c�������¶� d������SO3�����ʵ�����
��6����˵���÷�Ӧ�Ѿ��ﵽƽ��״̬���ǣ� ��
a�� v��SO3����2v��O2�� b��������ѹǿ���ֲ���
c��v�棨SO2��=2v����O2�� d���������������ʵ��ܶȱ��ֲ���
��7��Ϊʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ����ǣ� ��
a����ʱ�����SO3���� b���ʵ������¶�
c������O2��Ũ�� d��ѡ���Ч�Ĵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��ѧ��Ӧԭ���ڿ��к��������й㷺Ӧ�á�
��1�����á���ѧ����ת�Ʒ����Ʊ�TaS2���壬�������·�Ӧ��
TaS2��s����2I2��g�� TaI4��g����S2��g������H>0��I��
TaI4��g����S2��g������H>0��I��
��Ӧ����ƽ�ⳣ������ʽK��________����K��1����ij���������м���1 mol I2��g��������TaS2��s����I2��g����ƽ��ת����Ϊ________��
��2����ͼ��ʾ����Ӧ������ʯӢ��չ��н��У������¶�ΪT2��һ�˷���δ�ᴿ��TaS2��ĩ������I2��g����һ��ʱ������¶�ΪT1��һ�˵õ��˴���TaS2���壬���¶�T1________T2���>����<����������������Ӧ��ϵ��ѭ��ʹ�õ�������________��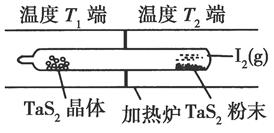
��3������I2�������Կɲⶨ��������ĺ����������ǽ������е���ת����H2SO3��Ȼ����һ��Ũ�ȵ�I2��Һ���еζ�������ָʾ��Ϊ________���ζ���Ӧ�����ӷ���ʽΪ______________________��
��4��25��ʱ��H2SO3 HSO3-��H���ĵ��볣��Ka��1��10��2mol��L��1������¶���NaHSO3ˮ�ⷴӦ��ƽ�ⳣ��Kh��________mol��L��1������NaHSO3��Һ�м���������I2������Һ��
HSO3-��H���ĵ��볣��Ka��1��10��2mol��L��1������¶���NaHSO3ˮ�ⷴӦ��ƽ�ⳣ��Kh��________mol��L��1������NaHSO3��Һ�м���������I2������Һ��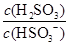 ��________���������С�����䡱����
��________���������С�����䡱����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�����仯�����ڹ�ũҵ������������������Ҫ���á�
��1����T��ʱ����0��6molH2��0��4molN2�����ݻ�Ϊ2 L���ܱ�������(ѹǿΪmPa)������Ӧ��3H2+N2 2NH3 ��H<0���������¶Ȳ��䣬ij��ȤС��ͬѧ��÷�Ӧ������������ѹǿ��ʱ��仯��ͼ��ʾ��8 min�ڷ���NH3��ƽ����������Ϊ mol��L-1��min-1��
2NH3 ��H<0���������¶Ȳ��䣬ij��ȤС��ͬѧ��÷�Ӧ������������ѹǿ��ʱ��仯��ͼ��ʾ��8 min�ڷ���NH3��ƽ����������Ϊ mol��L-1��min-1��
��2������T��ʱ����0��6molH2��0��4molN2����һ�ݻ��ɱ���ܱ��� ���С�
�����и�����˵���÷�Ӧ�Ѵﵽƽ��״̬���� (�����)��
a��������N2��H2��NH3��Ũ��֮��Ϊl��3��2
b��3v��(N2)=v��(H2)
c��3v��(H2)=2v��(NH3)
d�����������ܶȱ��ֲ���
e�������������ƽ����Է�����������ʱ����仯
�ڸ������´ﵽƽ��ʱNH3������������⣨1��������NH3������������ (������С�����䡱)��
�۴ﵽƽ��ı�ijһ����ʹ��Ӧ���ʷ�������ͼ��ʾ�ı仯���� ������������� ��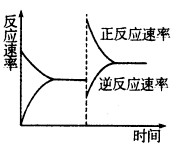
a�������¶ȣ�ͬʱ��ѹ
b�������¶ȣ�ͬʱ��ѹ
c�������¶ȡ�ѹǿ���䣬����Ӧ��Ũ��
d�������¶ȡ�ѹǿ���䣬��С������Ũ��
��3�����᳧��β�����е��������������ֱ���ŷŽ���Ⱦ������ �����ܽ��������ﻹԭΪ������ˮ���䷴Ӧ����Ϊ��
2NH3(g)+5NO2(g)=7NO(g)+3H2O(g)  H=-akJ��mol-1
H=-akJ��mol-1
4NH3(g)+6NO(g)=5N2(g)+6H2O(g)  H=-bkJ��mol-1
H=-bkJ��mol-1
��NH3ֱ�ӽ�NO2��ԭΪN2���Ȼ�ѧ����ʽΪ�� ��
����״����NO��NO2�������40��32L��������ˮ��ȫ���գ�������״���µ���42��56L���û��������NO��NO2�����֮��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��֪���淴Ӧ:A(g)��B(g) C(g)��D(g) ��H��0����ش���������:
C(g)��D(g) ��H��0����ش���������:
(1)��ij�¶��£���Ӧ�����ʼŨ�ȷֱ�Ϊ:c(A)="1" mol/L��c(B)="2.4" mol/L���ﵽƽ��ʱ��A��ת����Ϊ60%����ʱB��ת����Ϊ ��
(2)����Ӧ�¶Ƚ��ͣ���B��ת���ʽ� (���������С�����䡱)��
(3)����Ӧ�¶Ȳ��䣬��Ӧ�����ʼŨ�ȷֱ�Ϊc(A)="4" mol��L-1��c(B)=" a" mol��L-1���ﵽƽ���c(C)="2" mol��L-1����a= ��
(4)����Ӧ�¶Ȳ���,��Ӧ�����ʼŨ�ȷֱ�Ϊc(A)="c(B)=b" mol/L���ﵽƽ���c(D)= ��(������λ��Ч����)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��ҵ���������������ͼ���£� 
��ش��������⣺
��1���������������Ի�����Ϊԭ�ϣ������ڹ����������������Ϊԭ�ϣ������� ��
��2��������������Ӧ��ǰ�辻����ԭ���� ��
��3���ڴ���Ӧ����ͨ��ʹ�ó�ѹ���ڴ�������SO2��ת����Ϊ90%�����Dz��ַ�����Ҳ�ȡ��ѹ��������ȡSO3����ȡ��ѹ��ʩ��Ŀ�ij��˼ӿ췴Ӧ�����⣬������ ���Ӷ��������Ч�� ��
��4����ҵ�����г��ð����ᷨ����β�������Դﵽ������Ⱦ���������õ�Ŀ�ġ��û�ѧ����ʽ��ʾ�䷴Ӧԭ���� ��
��5�������Ṥҵ�⣬�������ҵ������������صĹ�ҵ������������ȷ���� �� 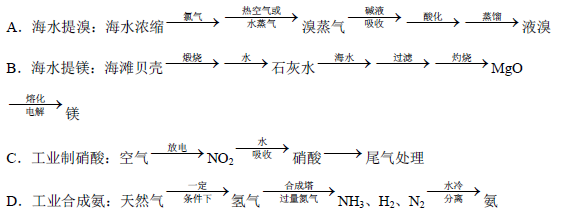
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��ij�ܱ������м���0.3mol A��0.1mol C��һ����������B�������壬��һ�������·�����Ӧ��������Ũ����ʱ��仯��������ͼ��ʾ��������ͼΪt2ʱ�̺�ı�������������ƽ����ϵ��������ʱ��仯�������t2��t5�ĸ��ζ����ı�һ��������������������ͬ��t3��t4��Ϊʹ�ô�����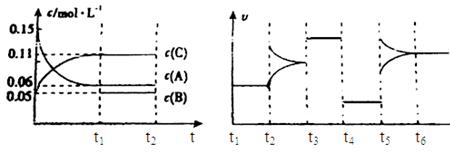
��1����t1��15s����t0��t1����CŨ�ȱ仯��ʾ�ķ�Ӧ����Ϊv��C���� mol/(L?s)��
��2����t2��t3�Σ�C�����������С���˽�v�� v��(����ڡ�����С�ڡ����ڡ�)
��3��B����ʼ���ʵ���Ϊ mol��
��4��t1ʱ�̣�ƽ�ⳣ��K�� ��
��5��t5��t6��������A�����ʵ�������С0.03mol�����˹����������������Ƚ�������Ϊa KJ��д���÷�Ӧ���Ȼ�ѧ����ʽ ��
��6����t2ʱ�̺�ͼ��仯����ͼ����ı�����Ϊ 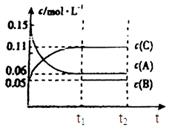
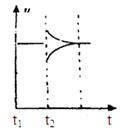
a�����º�ѹ�£�����2��1����������������B��C
b�����º�ѹ�£�����0.24mol A��0.06mol B��0.14mol C
c�����º�ѹ�£�����0.12mol A��0.1mol B��0.22mol C
d�����º�ѹ�£�����0.14mol B��0.30mol C
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com