
| A. | 0.44s | B. | 1s | C. | 7.33s | D. | 2s |
分析 先依据氢气的反应速率,结合速率之比等于化学计量数之比计算出v(NH3),再根据t=$\frac{△c}{v}$计算时间.
解答 解:H2 表示的平均速率v(H2 )=0.45mol/(L?s),
利用速率之比等于化学计量数之比,所以v(NH3)=$\frac{2}{3}$v(H2 )=$\frac{2}{3}$×0.45mol/(L?s)=0.3mol/(L?s),
氨的浓度增加了0.6mol/L,即△c(NH3)=0.6mol/L,
所以反应所经历的时间为 $\frac{0.6mol/L}{0.3mol/L•s}$=2s,
故选D.
点评 本题考查化学反应速率的有关计算,难度不大,注意对公式的理解与灵活运用.


 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:选择题
| A. | 上海世博会很多场馆的外墙使用的非晶体薄膜,以充分利用天阳能,体现低碳经济 | |
| B. | 金属的电化学防护措施有牺牲阳极的阴极保护法和外加电流的阴极保护法 | |
| C. | 若在水果贮藏室中,放几块被KMnO4溶液浸透过的“砖块”,可延长水果保存时间 | |
| D. | 常温时,某可逆反应的平衡常数越大则其反应速率就越快 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
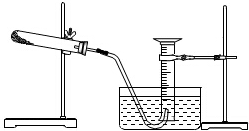 某同学完成以胆矾为原料制取氧化铜固体实验,并用氧化铜和氯酸钾的混合物制取氧气,测量生成氧气的体积.试回答:
某同学完成以胆矾为原料制取氧化铜固体实验,并用氧化铜和氯酸钾的混合物制取氧气,测量生成氧气的体积.试回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
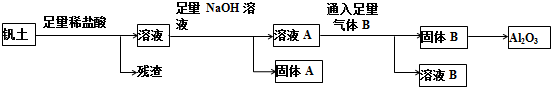
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
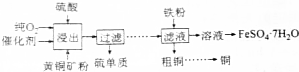
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应是分解反应 | B. | 该反应的熵增效应大于焓变效应 | ||
| C. | 该反应是熵减反应 | D. | 该反应是放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com