
第四层为最外层时,该电子层最多容纳的电子数目是
| A.2个 | B.8个 | C.18个 | D.32个 |
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:单选题
下列说法正确的是
| A.云、雾、烟都属于胶体,其分散剂都是空气 |
| B.新制氯水中的所有物质都是电解质 |
| C.水晶项链和餐桌上的瓷盘都是硅酸盐制品 |
| D.制造光导纤维的原料是晶体硅 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是
A.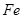 与稀 与稀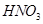 、稀 、稀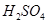 反应均有气泡产生,说明 反应均有气泡产生,说明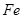 与两种酸均发生置换 与两种酸均发生置换 |
B.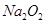 中阴阳离子数数目之比为1:1 中阴阳离子数数目之比为1:1 |
C.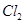 与 与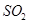 均能使品红褪色,说明二者均有氧化性 均能使品红褪色,说明二者均有氧化性 |
D.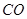 能够与人体里的血红蛋白结合,造成人体缺氧中毒 能够与人体里的血红蛋白结合,造成人体缺氧中毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
NH3.H2O.CH4三分子中键角大小顺序正确的是
| A.NH3>H2O>CH4 | B.CH4>NH3>H2O |
| C.CH4>H2O>NH3 | D.H2O>CH4>NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在2升的密闭容器中,发生以下反应:2A(g)+B(g)  2C(g)+D(g)。若最初加入的A和B都是4 mol,在前10秒钟A的平均反应速率为0.12 mol/(L·s),则10秒钟时,容器中B的物质的量是
2C(g)+D(g)。若最初加入的A和B都是4 mol,在前10秒钟A的平均反应速率为0.12 mol/(L·s),则10秒钟时,容器中B的物质的量是
| A.1.6 mol | B.2.8 mol | C.2.4 mol | D.1.2 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(14分)某学生用0.1000 mol·L-1的NaOH标准溶液滴定未知浓度的盐酸,其操作可分解为如下几步:
A.移取20 mL待测盐酸溶液注入洁净的锥形瓶,并加入2~3滴酚酞;
B.用标准溶液润洗滴定管2~3次;
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液;
D.取标准NaOH溶液注入碱式滴定管至刻度0以上2~3 cm;
E.调节液面至0或0以下刻度,记下读数;
F.把锥形瓶放在滴定管的下面,用标准NaOH溶液滴定至终点并记下滴定管液面的刻度。
就此实验完成填空:
(1)正确操作步骤的顺序是(用序号字母填写)______________________________。
(2)上述B步骤操作的目的是_______________________________________。
(3)实验中用左手控制活塞,眼睛注视 ___________________,直至滴定终点。判断到达终点的现象是________________________________。
(4)某学生根据3次实验分别记录有关数据如下表:
| 滴定 次数 | 待测溶液的体积(mL) | 0.100 0 mol·L-1NaOH的体积(mL) | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积(mL) | ||
| 第一次 | 20.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 20.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 20.00 | 0.22 | 26.31 | 26.09 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com