
| A. | 只有③④ | B. | 只有③⑤ | C. | 只有①③⑤ | D. | 只有①②④ |
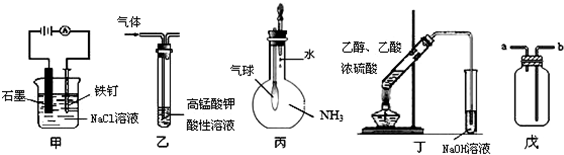
分析 ①铁钉与原电池正极相连,为电解池的阳极,加快了铁的腐蚀;
②装置乙中乙烯、甲醛均能被高锰酸钾氧化;
③装置丙中氨气极易溶于水,烧瓶中气压变小,则气球变大;
④装置丁中乙酸乙酯在NaOH溶液中水解;
⑤装置戊为多用瓶,a端进气可收集H2,b端进气可收集CO2、Cl2、HCl、NO2等气体.
解答 解:①装置甲中铁为阳极,加快了Fe的腐蚀,不能防止铁钉被腐蚀,故①错误;
②装置乙中甲醛、乙烯均能被高锰酸钾氧化,无法达到除杂的目的,故②错误;
③装置丙中氨气极易溶于水,烧瓶中气压变小,则气球变大,可检验NH3气体在水中的溶解性,故③正确;
④装置丁中乙酸乙酯在NaOH溶液中水解,应选择饱和的碳酸钠溶液,故④错误;
⑤装置戊为多用瓶,a端进气可收集密度比空气小的气体,如H2,b端进气可收集密度比空气大的,如CO2、Cl2、HCl、NO2等气体,故⑤正确;
故选B.
点评 本题考查化学实验方案的评价,题目难度中等,涉及电化学腐蚀、除杂、气体的收集、有机化学实验等,注重实验操作及实验原理的考查,有利于提高学生的分析能力及化学实验能力.


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 氯化氢溶于水能电离出H+、Cl-,所以氯化氢是离子化合物 | |
| B. | 碘晶体受热转变成碘蒸气,吸收的热量用于克服碘原子之间的作用力 | |
| C. | 烧碱固体溶于水的过程中,共价键被破坏 | |
| D. | 有机化合物CH3CH2NO2与H2N-CH2-COOH是同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器中的压强不变 | B. | 混合物的平均相对分子质量不变 | ||
| C. | 各组分的浓度不变 | D. | 混合气体的密度不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无法比较 | B. | V(B)=0.6 mol/(L•min) | ||
| C. | V(AB3)=0.5 mol/(L•min) | D. | V(A)=0.4mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高级脂肪酸甘油酯相对分子质量很大,属于高分子化合物 | |
| B. | 缩聚反应的单体至少有两种物质 | |
| C. | 线性高分子的长链上可以带支链 | |
| D. | 电木具有热塑性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com