
(14分)A、B、C是常见短周期元素的单质,常温下D为无色液体,E是一种常见的
温室气体。其转化关系如图所示(反应条件和部分产物略去)。试回答:
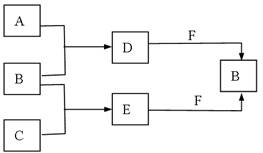
(1)F的电子式为 ;
(2)少量的金属单质铝与D和F混合,写出反应的离子方程式 。
(3)D2mol、E 2mol与3molF在密闭容器中充分反应,所得固体成分为 ;其相应的物质的量为 。
科目:高中化学 来源: 题型:阅读理解
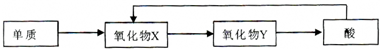


| ||
| △ |
| ||
| △ |
| T/K | 303 | 313 | 323 |
| CA2生成量/(10-1mol) | 4.3 | 5.9 | 6.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:


 AlO2-+H++H2O
AlO2-+H++H2O AlO2-+H++H2O
AlO2-+H++H2O查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A元素的原子半径最 小;B元素的最高价氧化物对应水化物与其氢化物能生成盐;D与A同主族,且与E同周 期;E元素原子的最外层电子数是其次外层电子数的
A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A元素的原子半径最 小;B元素的最高价氧化物对应水化物与其氢化物能生成盐;D与A同主族,且与E同周 期;E元素原子的最外层电子数是其次外层电子数的| 3 | 4 |
查看答案和解析>>
科目:高中化学 来源:2010年重庆理科测试模拟试卷(一)化学部分 题型:填空题
(15分)
现有A、B、C、D四种常见的短周期主族元素,其原子序数依次增大.其中A、B是同周期相邻元素,且A单质及其氢化物是重要的工业生产原料;C、D是同周期元素,且在该周期中,分别为原子半径最大和最小的元素,C、D最外层电子数之和与B的原子序数相等,回答下列问题:
(1)B元素的名称为 ,C元素在周期表中位于第 周期第 族.
(2)工业上由A单质合成其氢化物的化学反应方程式为: .
(3)当今工业电解CD饱和水溶液的装置名称是 ,阳极电极反应式为 ,溶液的pH将 (填“增大”、“减小”或“不变”),若有1mol电子转移,生成气体体积之和是 L(标准状况下).
查看答案和解析>>
科目:高中化学 来源:2013-2014学年山东省济南市高三3月模拟考试理综化学试卷(解析版) 题型:填空题
A、B、C是中学化学中常见的三种元素(A、B、C代表元素符号)。A位于元素周期表中第4周期,其基态原子最外层电子数为2且内层轨道全部排满电子。短周期元素B的一种常见单质为淡黄色粉末。元素C的原子最外层电子数是其内层电子数的3倍。
(1)在第3周期中,第一电离能大于B的元素有??? 种;
A与B形成晶体的晶胞如图所示,该晶胞实际拥有Bn-的数目为???????

(2)B的氢化物(H2B)分子的空间构型为 ????????? ;在乙醇中的溶解度:s(H2C)>s(H2B),其原因是???????? 。
(3)B与C可形成BC42-
①BC42-中,B原子轨道的杂化类型是??? 。
②人们将价电子数和原子数分别相同的不同分子、离子或原子团称为等电子体。与BC42-互为等电子体的分子的化学式为? ??? ? (写出一种即可)。
(4)A的氯化物与氨水反应可形成配合物[A(NH3)4]Cl2,l mol该配合物中含有 键的物质的量为??? mol。
键的物质的量为??? mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com