
科目:高中化学 来源: 题型:
(1)有关研究表明CO2在大气中含量增大,导致地球表面的温度升高,即温室效应。为了控制温室效应,各国科学家提出了不少方法和设想。有人设想将CO2分子液化或制成干冰,封存于地下或海底,以减小大气中CO2的浓度。为使CO2液化,可采用的措施是________。
A.减压、升温  B.增压、升温
B.增压、升温
C.减压、降温 D.增压、降温
快速、有效地减缓大气中的CO2,可采用的生态学措施是____________。
A.使用天然气等燃料 B.控制全球人口增长
C.植树造林,保护森林 D.立即停止煤和石油的燃烧
(2)将一定体积的CO2通入到一定浓度的NaOH溶液中,为了测定其溶液的成分,向该溶液中逐滴加入1 mol·L-1的盐酸。所加入盐酸的体积与产生CO2气体的体积(标准状况)的关系如图所示。
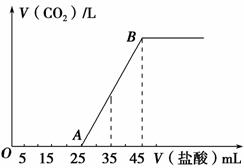

①写出OA段所发生反应的离子方程式_____________________________。
②当加入35 mL盐酸时,产生CO2的体积为____________mL(标准状况)。
③溶液中所含的物质有_______________________,其物质的量之比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
超细氧化镍(NiO)是一种功能材料,已被广泛用于电池电极、催化剂、半导体、玻璃染色剂等方面。工业上常以Ni(NO3)2·6H2O和尿素[CO(NH2)2]为原料制备。
(1)Ni2+的基态核外电子排布式为 。
(2)与NO3-离子互为等电子体的一种分子的分子式为 ,该分子的空间几何构型为 。
(3)尿素分子中碳原子的杂化方式为 ,1mol尿素分子中含有的σ键数为 。
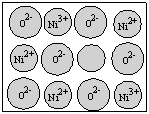 (4)NiO(氧化镍)晶体的结构与NaCl相同,但天然的和绝大部分人工制备的晶体都存在各种缺陷,例如在某种NiO晶体中就存在如右图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+-所取代。其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生了变化。经测定某氧化镍样品中Ni3+与Ni2+的离子数之比为6∶91。若该晶体的化学式为NiXO,则X= 。
(4)NiO(氧化镍)晶体的结构与NaCl相同,但天然的和绝大部分人工制备的晶体都存在各种缺陷,例如在某种NiO晶体中就存在如右图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+-所取代。其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生了变化。经测定某氧化镍样品中Ni3+与Ni2+的离子数之比为6∶91。若该晶体的化学式为NiXO,则X= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
由乙醛和乙酸乙酯组成的混合物中,若含碳的质量分数为A%,则此混合物中含氢的质量分数为 ( )
A.6A% B.A/6% C.10A% D.(100-7A/6)%
查看答案和解析>>
科目:高中化学 来源: 题型:
已知有机化合物 A、B、C、D、E存在下图所示转化关系,且C能跟NaHCO3发生反应,C和D的相对分子质量相等,E为无支链的化合物。
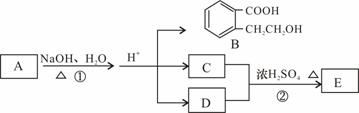 |
请回答下列问题:
(1)已知E的相对分子质量为102,其中碳、氢两种元素的质量分数分别为58.8%、9.8%,其余为氧,则E的分子式为 。
(2)B在一定条件下可以发生缩聚反应生成某高分子化合物,此高分子化合物的结构简式为 。
(3)C的核磁共振氢谱中有 个峰;D也可以由卤代烃F在NaOH溶液中加热来制取,写出此反应的化学方程式 。
(4)A的结构简式是 。
(5)B有多种同分异构体,请写出一种同时符合下列四个条件的结构简式:
。
a.能够发生水解 b.能发生银镜反应
c.能够与FeCl3溶液显紫色 d.苯环上的一氯代物只有一种
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于甲烷、乙烯、乙醇、乙酸的说法中,不正确的是 ( )
A.乙烯可以使溴水褪色,发生加成反应
B.甲烷和氯气光照条件下反应,反应类型为取代反应
C.乙醇在铜做催化剂并加热条件下生成乙醛,发生还原反应
D.生活中可以用食醋除去水壶中的水垢,主要是利用了食醋中醋酸的酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
化学中存在一些守恒或平衡原理,下列叙述正确的是 ( )
A.根据质量(原子)守恒定律,某物质完全燃烧的产物是CO2和H2O则该物
质一定是烃
B.根据能量守恒定律,所有化学反应的反应物的总能量一定等于生成物的
总能量
C.根据电子守恒定律,原电池中负极反应失电子数一定等于正极反应得电
子数
D.根据化学平衡原理,可逆反应的正反应速率在任何时刻一定等于逆反应
速率
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素A、B、C、D原子序数依次增大,且C元素最高价氧化物对应的水化物能 电离出电子数相等的阴、阳离子。A、C位于同一主族 ,A为非金属元素,B的最外层 电子数是次外层电子数的3倍,B、C的最外层电子数之和与D的最外层电子数相等。E 单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏。请回答下列问题:
,A为非金属元素,B的最外层 电子数是次外层电子数的3倍,B、C的最外层电子数之和与D的最外层电子数相等。E 单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏。请回答下列问题:
(1)C的最高价氧化物对应水化物的化学式为________________________ ______,
______,
其中含有的化学键类型为___ __________________________________________。
__________________________________________。
(2)由上述A、B、C、D四种 元素中的三种组
元素中的三种组 成某种盐,水溶液显碱性,是家用消毒剂 的主要成分。将该盐溶液滴入KI淀粉溶液中,溶液变为蓝色,则反应的离子方程式为 ________________________________________________________________________。
成某种盐,水溶液显碱性,是家用消毒剂 的主要成分。将该盐溶液滴入KI淀粉溶液中,溶液变为蓝色,则反应的离子方程式为 ________________________________________________________________________。
(3)E元素与D元素可形成ED2和ED3两种化合物,下列说 法正确的是________(填序 号)。
法正确的是________(填序 号)。
①保存ED2溶液时,需向溶液中加入少量E单质
②ED2只能通过置换反应生成,ED3只能通过 化合反应生成
化合反应生成
③铜片、碳棒和ED3溶液组成原电池,电子由铜片沿导线流向碳棒
④向淀粉碘化钾溶液和苯酚溶液中分别滴加几滴ED3的浓溶液,原无色溶液都变成紫色
查看答案和解析>>
科目:高中化学 来源: 题型:
下列排列有错误的是( )
A.粒子半径:F->Na+>Mg2+>Al3+B.稳定性:HI>HBr>HCl>HF
C.酸性:H4SiO4<H3PO4<H2SO4<HClO4
D.碱性:Al(OH)3<Mg(OH)2<Ca(OH)2<KOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com