
| A. | 反应热就是反应发出的热量 | |
| B. | 由C(s)+$\frac{1}{2}$O2(g)═CO(g)的反应热为110.5kJ•mol-1,可知碳的燃烧热为110.5 kJ•mol-1 | |
| C. | 反应热的大小与反应物所具有的能量和生成物所具有的能量无关 | |
| D. | 1mol NaOH分别和1mol CH3COOH、1mol HNO3反应放出的热量:CH3COOH<HNO3 |
分析 A、反应热是指反应过程中所放出或吸收的热;
B.燃烧热是指1mol可燃物完全燃烧生成稳定氧化物放出的热量;
C.化学反应的焓变决定于反应物与生成物的能量差;
D.强酸强碱稀溶液完全反应生成1mol水放热的热量为中和热,醋酸是弱酸存在电离平衡,电离过程是吸热过程;
解答 解:A、反应过程中吸收的热都也是反应热,故A错误;
B.碳的燃烧热是弱酸生成二氧化碳放出的热量,一氧化碳是不稳定的氧化物,故B错误;
C.化学反应的焓变决定于反应物与生成物的能量差,反应热的大小与反应物所具有的能量和生成物所具有的能量有关,故C错误;
D.醋酸是弱酸存在电离平衡,电离过程是吸热过程,1mol NaOH分别和1mol CH3COOH、1mol HNO3反应放出的热量:CH3COOH<HNO3,故D正确;
故选D.
点评 本题考查了化学反应能量变化,燃烧热、中和热概念的理解应用,注意反应焓变的计算方法,题目较简单.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 上述钛原子中,中子数不可能为22 | |
| B. | 钛元素在周期表中处于第四周期ⅡB族 | |
| C. | 钛原子的外围电子层排布为3d24s2 | |
| D. | 钛元素位于元素周期表的d区,是过渡元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 弱酸 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数Ka | 1.8×10-5 | 4.9×10-10 | Ka1=4.3×10-7; Ka2=5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 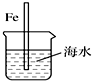 图中,插入海水中的铁棒,越靠近底端腐蚀越严重 | |
| B. |  图中,发生吸氧腐蚀 | |
| C. | 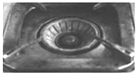 图中,燃烧灶的中心部位容易生锈,主要是由于高温下铁发生化学腐蚀 | |
| D. | 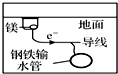 图中,用牺牲镁块的方法来防止地下钢铁管道的腐蚀,镁相当于原电池的正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氟利昂(CCl2F2)因破坏大气臭氧层,会导致“温室效应” | |
| B. | 生活污水中所含的氮、磷化合物是植物营养素,但会导致水体污染 | |
| C. | 废旧电池的回收,其主要目的是为了保护环境 | |
| D. | 淀粉餐具被认为是最有发展前景的一次性餐具,可有利于保护环境 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com