
| A. | ①②③④ | B. | ①③②④ | C. | ④③②① | D. | ④③①② |
科目:高中化学 来源: 题型:选择题
| A. | 实验室少量金属钠保存在煤油中 | |
| B. | 从锂到铯,金属性逐渐减弱 | |
| C. | 金属钠与水反应时放出氢气 | |
| D. | 从锂到铯,单质与水反应越来越剧烈 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2通常用于通讯行业 | B. | 硅胶常用于食品袋中的干燥剂 | ||
| C. | SO2可用于食品行业的漂白剂 | D. | 氧化铝可用于制造坩埚 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应中NF3是氧化剂,H2O是还原剂 | |
| B. | NF3在潮湿空气中泄漏会产生无色气体 | |
| C. | 反应中还原剂与氧化剂的物质的量之比为1:2 | |
| D. | 若反应中生成0.1 mol HNO3,则反应共转移0.1 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KAl(SO4)2•12H2O可除去碱性废水中的悬浮颗粒 | |
| B. | 漂白粉的主要成分为氯化钙 | |
| C. | 实验室可用浓硫酸干燥氨气和氯气 | |
| D. | 实验室可用NaOH溶液处理NO和CO废气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH═CH2与HCl加成 | |
| B. | CH3CH2CH2Cl在碱性溶液中水解 | |
| C. | CH2═CH-CH═CH2与H2按物质的量之比为1﹕1进行反应 | |
| D. | 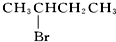 与NaOH的醇溶液共热 与NaOH的醇溶液共热 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com