
(1)方案一:选择的试剂(只允许一种试剂)_________________________,观察到的现象________________________。
(2)方案二:选择的试剂(只选两种试剂)____________________________,观察到的现象____________________。
(3)方案三:选择试剂(只选两种试剂)_________________________________________,观察到的现象______________________。
(4)除上述方案外,若还有可行方案,请增写其中的一种(若无,此小题免答)。选择试剂
__________,观察到的现象______________________________。
解析:因为亚硝酸为极不稳定的弱酸,3HNO2====2NO↑+HNO3+H2O,而2NO+O2====2NO2。(1)若取试样加入稀硫酸中,若产生无色气体并在空气中变为红棕色的是亚硝酸钠,另一者为氯化钠。(2)因亚硝酸钠水解显碱性,而氯化钠不水解,溶液呈中性,故可用水和酚酞两种试剂鉴别亚硝酸钠和氯化钠。(3)因亚硝酸钠在酸性条件下具有较强的氧化性(可将Fe2+氧化为Fe3+),能将I-氧化为I2而使淀粉变蓝色,故可用稀硫酸和碘化钾淀粉溶液鉴别亚硝酸钠和氯化钠。(4)因为![]() 不与Ag+作用,所以也可用稀硝酸和硝酸银溶液来进行鉴别。
不与Ag+作用,所以也可用稀硝酸和硝酸银溶液来进行鉴别。
答案:(1)② 无色气体变红棕色
(2)⑤⑥ 溶液呈红色
(3)②④ 溶液变蓝色
(4)①③ 白色沉淀


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
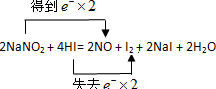
经常有人因误食亚硝酸钠(NaNO2)而中毒。原因是NaNO2像食盐一样既有咸味,又有很强毒性。已知亚硝酸钠能发生如下反应:2NaNO2 + 4HI= 2NO + I2 + 2NaI + 2H2O
(1)在此反应中,氧化剂是________(填化学式),氧化产物是___________(填化学式)。
(2)用双线桥表示电子转移的情况__________________。
(3)若有1mol还原剂被氧化,则在此反应中发生转移的电子数目为____ ___。
查看答案和解析>>
科目:高中化学 来源:2011-2012年浙江省高一上学期期中考试化学试卷 题型:选择题
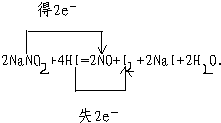
经常有人因误食亚硝酸钠(NaNO2)而中毒。原因是NaNO2像食盐一样既有咸味,又有很强毒性。已知亚硝酸钠能发生如下反应:2NaNO2 + 4HI= 2NO + I2 + 2NaI + 2H2O
(1)在此反应中,氧化剂是________(填化学式),氧化产物是___________(填化学式)。
(2)用双线桥表示电子转移的情况__________________。
(3)若有1mol还原剂被氧化,则在此反应中发生转移的电子数目为____ ___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com