
 ������ϵͳ��������д�����и���������
������ϵͳ��������д�����и���������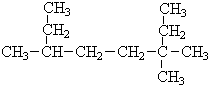 ��3��3��6-��������
��3��3��6-������������ �����ɽṹ��ʽ��֪��������8��Cԭ�ӣ�����3������
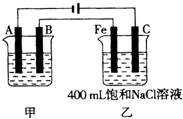
����1�����������õ��ԭ�������϶���������ӦΪ��������Ϊ��������Ϊ���ʳ��ˮ�������������������������ƣ�
��2����������������4.32g��n��Ag��=$\frac{4.32g}{108g/mol}$=0.04mol���Ҳ���������������������2Cl--2e-=Cl2������ϵ缫����ʽ���㣻
��3������Ϊǿ�������Σ�ˮ��ʼ��ԣ�����������ˮ�⣮
��� �⣺�����ɽṹ��ʽ��֪��������8��Cԭ�ӣ�����3����������Ϊ3��3��6-�������飬�ʴ�Ϊ��3��3��6-�������飻
����1�����������õ��ԭ�������϶���������ӦΪ��������Ϊ��������Ϊ���ʳ��ˮ�������������������������ƣ��缫����ʽΪ2Cl-+H2O$\frac{\underline{\;���\;}}{\;}$Cl2��+H2��+2OH-��
�ʴ�Ϊ��Fe�� ������2Cl-+H2O$\frac{\underline{\;���\;}}{\;}$Cl2��+H2��+2OH-��
��2����������������4.32g��n��Ag��=$\frac{4.32g}{108g/mol}$=0.04mol���Ҳ���������������������2Cl--2e-=Cl2������Ӧ����0.02mol���������Ϊ0.02mol��22.4L/mol=0.448L=448mL��
�ʴ�Ϊ��448��
��3������Ϊǿ�������Σ�ˮ��ʼ��ԣ�����ʽΪS2-+H2O?HS-+OH-������������ˮ�⣬�ʴ�Ϊ��NaOH��S2-+H2O?HS-+OH-��
���� ���⿼���Ϊ�ۺϣ��漰�л����������Ϊ��Ƶ���㣬������ѧ���ķ��������������Ŀ��飬ע�����յ��ԭ�����缫��Ӧʽ����д����������������ѧ���ķ���������������ʵ�����������


 ��ĩ��ϰ���ϵ�д�
��ĩ��ϰ���ϵ�д� ����ѧ�䵥Ԫ������ĩר����100��ϵ�д�
����ѧ�䵥Ԫ������ĩר����100��ϵ�д� �Ƹ�360�ȶ����ܾ�ϵ�д�
�Ƹ�360�ȶ����ܾ�ϵ�д� ���⿼����Ԫ���Ծ�ϵ�д�
���⿼����Ԫ���Ծ�ϵ�д� ��У���˳�̾�ϵ�д�
��У���˳�̾�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Q1��Q2��Q2=2Q3 | B�� | Q1=Q2=Q3 | C�� | Q1��Q2��Q3=$\frac{{Q}_{1}}{2}$ | D�� | ���Ƚ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
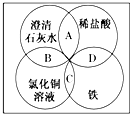 ����ϡ���ᡢ����ʯ��ˮ���Ȼ�ͭ��Һ�dz��л�ѧ�г��������ʣ��������ʼ�ķ�Ӧ��ϵ��ͼ��ʾ��ͼ����Բ�ཻ���֣�A��B��C��D����ʾ���ʼ�ķ�Ӧ�����ж�Ӧ�ĸ���Ӧ���͵�˵����ȷ���ǣ�������
����ϡ���ᡢ����ʯ��ˮ���Ȼ�ͭ��Һ�dz��л�ѧ�г��������ʣ��������ʼ�ķ�Ӧ��ϵ��ͼ��ʾ��ͼ����Բ�ཻ���֣�A��B��C��D����ʾ���ʼ�ķ�Ӧ�����ж�Ӧ�ĸ���Ӧ���͵�˵����ȷ���ǣ�������| A�� | ���ֽⷴӦ�����ֽⷴӦ�����Ϸ�Ӧ���û���Ӧ | |
| B�� | �кͷ�Ӧ���û���Ӧ�����ֽⷴӦ���û���Ӧ | |
| C�� | ���ֽⷴӦ�����ֽⷴӦ���û���Ӧ���û���Ӧ | |
| D�� | �ֽⷴӦ�����ֽⷴӦ���û���Ӧ���û���Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���³�ѹ�£���0.5molHI�����0.5molCl2��Ϻ�����ķ�������ΪNA | |
| B�� | ��״���£�11.2L��SO3����������Ϊ0.5NA | |
| C�� | ����Ϊ7.8g��Na2S��Na2O2��ɵĹ��������к��е�������������Ϊ0.1NA | |
| D�� | ij�ܱ�����ʢ��0.1molN2��0.3molH2����һ�������³�ַ�Ӧ��ת�Ƶ��ӵ���ĿΪ0.6NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ����ͼ��ʾװ�ý���ʵ�飬��Һ��A��μ��뵽����B�У��ش��������⣺
����ͼ��ʾװ�ý���ʵ�飬��Һ��A��μ��뵽����B�У��ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 24�� | B�� | 28�� | C�� | 32�� | D�� | 40�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com