
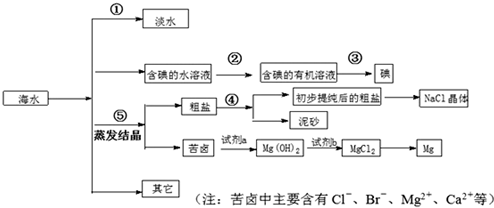
分析 海水中还含有大量的电解质,它们电离产生Cl-、Br-(溴离子)、SO42-、Na+、Mg2+、Ca2+等,
海水经过蒸馏,可得到淡水;
碘易溶于有机溶剂,可加入苯或四氯化碳进行萃取,然后蒸馏可得到碘;
海水经蒸发结晶得到粗盐,粗盐经提纯化学处理后过滤可得到氯化钠;
海水中含有氯化镁,加入石灰水,可生成氢氧化镁沉淀,过滤后在沉淀中加入盐酸可生成氯化镁,经蒸发、结晶和脱水后可得氯化镁,电解熔融的氯化镁可得金属镁,以此解答该题.
解答 解:(1)步骤①为海水的淡化,可用蒸馏操作分离,②为碘的萃取和分液,④为过滤,粗盐经提纯化学处理后过滤可得到氯化钠溶液,
故答案为:蒸馏; 萃取分液; 过滤;
(2)步骤②分离提纯方法为萃取,需要选用主要玻璃仪器为分液漏斗、烧杯,故答案为:分液漏斗、烧杯;
(3)镁离子会与氢氧根离子、碳酸根离子生成沉淀,钙离子会与碳酸根离子生成沉淀,硫酸根离子会与钡离子生成沉淀,过滤后加入盐酸可以除去过量的碳酸钠和氢氧化钠,需要依次加入稍过量的NaOH、BaCl2 、Na2CO3、过滤、在滤液中加入盐酸至不再有气体生成,将所得溶液加热浓缩、冷却结晶,得到精盐,Na2CO3 溶液滴加顺序是在加在BaCl2溶液之后,是为了除去过量的BaCl2,加在盐酸之前,可用盐酸除去过量的Na2CO3,确保得到的NaCl不含杂质
故答案为:Na2CO3 溶液滴加顺序是在加在BaCl2溶液之后,是为了除去过量的BaCl2,加在盐酸之前,可用盐酸除去过量的Na2CO3,确保得到的NaCl不含杂质.
点评 本题考查了混合物除杂的实验方案分析,氧化还原反应的强弱规律应用,离子方程式的书写方法等知识,为高频考点,侧重于学生的分析能力和实验能力的考查,体现化学来源于生产、生活,又服务于生产、生活的理念,题目难度中等.


 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 放电时负极上I-被氧化 | |
| B. | 充电时Li+从阳极区移向阴极区 | |
| C. | 充电时阴极反应为:LiOH+e-═Li+OH- | |
| D. | 放电时正极反应为:O2+2H2O+4Li++4e-═4LiOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 食品袋 | B. | 甲苯 | C. | 苯 | D. | 甲醛 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ①②④⑤ | C. | ②③④⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放出92 kJ热量 | B. | 吸收92 kJ热量 | C. | 放出46 kJ热量 | D. | 吸收46 kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4 | B. | C2H6 | C. | C3H8 | D. | C4H10 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏卫一高一上10月月考化学b卷(解析版) 题型:选择题
在配制一定物质的量浓度的溶液的实验中,下列操作正确的是
A. 将NaOH固体放在天平托盘的称量纸上,精确称量并放入烧杯中溶解后,立即注入容量瓶中
B. 将准确量取的18.4mol·L-1浓硫酸10mL,注入已盛有30 mL水的100 mL容量瓶中,加入至刻度线即可
C. 仰视容量瓶刻度线,看到液面超过了容量瓶刻度线,用胶头滴管吸出刻度线以上的溶液
D. 欲配制1000 mL 0.1 mol·L-1的盐酸,将稀释后的盐酸溶液全部转移到未经干燥的1000 mL的容量瓶中,加水至刻度线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com