
| 时间(s) | 20 | 40 | 60 | 80 | |
| n(NO2)/mol | 0.4 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.05 | n2 | 0.08 | 0.08 |
 N2O4的平衡常数将______(填“增大”、“减小”或“不变”)
N2O4的平衡常数将______(填“增大”、“减小”或“不变”) N2O4将______.(填“向左移动”、“向右移动”或“不移动”).
N2O4将______.(填“向左移动”、“向右移动”或“不移动”).
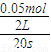 =0.00125mol?L-1?min-1,则v(NO2)=2v(N2O4)=2×0.00125mol?L-1?min-1=0.0025 mol?L-1?min-1,
=0.00125mol?L-1?min-1,则v(NO2)=2v(N2O4)=2×0.00125mol?L-1?min-1=0.0025 mol?L-1?min-1, N2O4
N2O4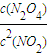 =
= =2.8(mol/L)-1,
=2.8(mol/L)-1, N2O4可知,0.4molNO2与0.2molN2O4相当,若在相同情况下最初向该容器充入的是四氧化二氮气体,要达到上述同样的平衡状态,四氧化二氮的起始浓度是
N2O4可知,0.4molNO2与0.2molN2O4相当,若在相同情况下最初向该容器充入的是四氧化二氮气体,要达到上述同样的平衡状态,四氧化二氮的起始浓度是 =0.1mol/L,故答案为:0.1mol/L;
=0.1mol/L,故答案为:0.1mol/L;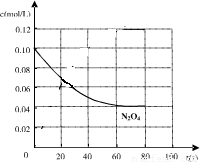 ;
;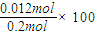 =60%,混合气体的平均摩尔质量与初始加入二氧化氮时混合气体的平均摩尔质量相等,
=60%,混合气体的平均摩尔质量与初始加入二氧化氮时混合气体的平均摩尔质量相等,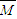 =
=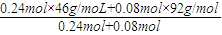 =57.5g.mol-1,故答案为:60%;57.5g.mol-1;
=57.5g.mol-1,故答案为:60%;57.5g.mol-1;

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在100℃时,将0.40mol二氧化氮气体充入2L抽空的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如下表数据:
在100℃时,将0.40mol二氧化氮气体充入2L抽空的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如下表数据:| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
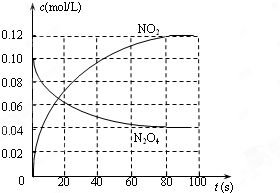

查看答案和解析>>
科目:高中化学 来源: 题型:
在100℃时,将0.40molNO2气体充入2L密闭容器中,每隔一段时间对该容器的物质进行测量,得到的数据如下表:
|
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
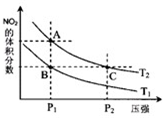 非金属元素氮有多种氧化物,如NO、NO2、N2O4等.
非金属元素氮有多种氧化物,如NO、NO2、N2O4等.| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
查看答案和解析>>
科目:高中化学 来源: 题型:
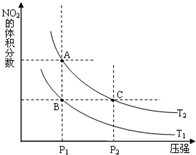 氮可形成多种氧化物,如NO、NO2、N2O4等,NO2和N2O4可以相互转化.
氮可形成多种氧化物,如NO、NO2、N2O4等,NO2和N2O4可以相互转化.| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com