
| 实验编号 | 实验温度/℃ | c(Na2S2O3)/mol•L-1 | c(H2SO4)/mol•L-1 |
| ① | 25 | 0.1 | 0.1 |
| ② | 25 | 0.1 | 0.2 |
| ③ | 50 | 0.2 | 0.1 |
| ④ | 50 | 0.1 | 0.1 |
分析 (1)探究温度对化学反应速率的影响,应选择浓度相同条件下的实验;要探究浓度对化学反应速率的影响,应选择温度相同条件下的实验;
(2)已知Na2S2O3溶液与Cl2反应时,1mol Na2S2O3转移8mol电子,氯气有强氧化性,将S2O32-氧化为2SO42-,根据这个关系写出离子方程式.
解答 解:(1)探究温度对化学反应速率的影响,应选择温度不两同,浓度相同条件下的实验,所以应选择①④;要探究浓度对化学反应速率的影响,应选择浓度不同,温度相同条件下的实验,所以应选择①②或③④;
故答案为:①④;①②或③④;
(2)已知Na2S2O3溶液与Cl2反应时,1mol Na2S2O3转移8mol电子,S2O32-中硫的化合价从+2价升高到+6价,1个S2O32-升高8价,得到2个SO42-,4个Cl2化合价降低8价,所以是4个Cl2将1个S2O32-氧化为2SO42-,根据这个关系写出离子方程式是:S2O32-+4Cl2+5H2O=2SO42-+8Cl-+10H+,
故答案为:S2O32-+4Cl2+5H2O=2SO42-+8Cl-+10H+.
点评 本题探究影响化学反应速率的因素,注意控制变量法讨论,第(2)题离子方程式的书写与量有关,用氧化还原反应中得失电子相等,化合价升降总数相等写出离子方程式.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
| 装置 | 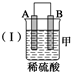 | 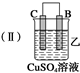 | 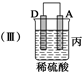 |
| 现象 | 二价金属A 不断溶解 | C的质 量增加 | A上有气 体产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子键是指阴阳离子间的静电引力 | |
| B. | 离子化合物是指只含有离子键的化合物 | |
| C. | 升高温度只能使吸热反应的速率增大,不能使放热反应的速率增大 | |
| D. | 粉碎固体反应物可以增大反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,反应的化学方程式为
,反应的化学方程式为 +HO-NO2$→_{△}^{浓硫酸}$
+HO-NO2$→_{△}^{浓硫酸}$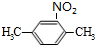 +H2O.
+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 氨水具有挥发性 | |
| B. | 1mol/L氨水溶液的pH=10 | |
| C. | 1mol/LNH4Cl溶液的pH=5 | |
| D. | 氨水与AlCl3溶液反应生成Al(OH)3沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验 混合溶液 | A | B | C | D | E | F |
| 4mol•L-1 H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 某学生用0.1000mol•L-1标准氢氧化钠溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
某学生用0.1000mol•L-1标准氢氧化钠溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有②③④ | B. | 只有②③⑦ | C. | 只有①③⑥ | D. | 只有⑤⑥⑧ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com