
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |


 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:高中化学 来源: 题型:
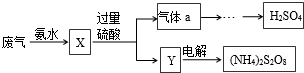
| A、X可能含有2种盐 |
| B、a是SO3 |
| C、Y中含NH4HSO4 |
| D、(NH4)2S2O8中S的化合价不可能为+7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 磺化煤(表达式为NaR)是一种钠离子型离子交换剂,它能与硬水中的Ca2+、Mg2+交换而将其除去,从而使水软化.现代海水的淡化方法是使海水按顺序通过两种离子交换剂,其流程如图所示.
磺化煤(表达式为NaR)是一种钠离子型离子交换剂,它能与硬水中的Ca2+、Mg2+交换而将其除去,从而使水软化.现代海水的淡化方法是使海水按顺序通过两种离子交换剂,其流程如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
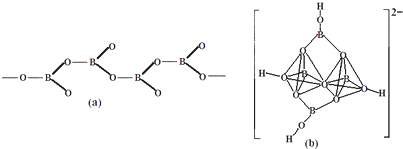
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙醇在一定条件下可以转化成乙醛、乙酸乙酯或CO2 |
| B、(NH4)2SO4溶液、CuSO4溶液和福尔马林都可使蛋白质变性 |
| C、乙烯和苯都能使酸性KMnO4溶液褪色 |
| D、煤的干馏、油脂的皂化和石油的分馏都属于化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、淀粉、油脂、蛋白质均为天然高分子化合物 |
| B、葡萄糖和果糖互为同分异构体,淀粉和纤维素也互为同分异构体 |
| C、羊毛、棉花、蚕丝、麻都是天然纤维 |
| D、1mol蔗糖完全水解可生成2mol葡萄糖 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com