
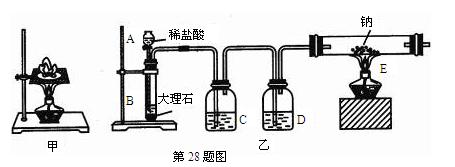
科目:高中化学 来源:不详 题型:填空题
| | NaOH溶液 | 银氨溶液 | 新制Cu(OH)2 | 金属钠 |
| A | 中和反应 | —— | 溶 解 | 产生氢气 |
| B | —— | 有银镜 | 加热后有红色沉淀 | 产生氢气 |
| C | 水解反应 | 有银镜 | 加热后有红色沉淀 | —— |
| D | 水解反应 | —— | —— | —— |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.SO2气体的还原性较强,不能使其通过浓硫酸干燥 |
| B.滴定管洗净后经蒸馏水润洗,即可注入标准液进行滴定 |
| C.用图1装置吸收多余的HCl气体 |
| D.用图2装置检验溴乙烷发生消去反应生成乙烯 |
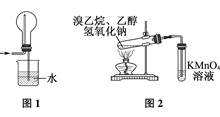
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 实验操作 | 实验目的或结论 |
| A | 向NaAlO2溶液中滴加饱和NaHCO3溶液,有白色沉淀产生 | 验证两者都发生了水解反应,且相互促进 |
| B | 苯酚溶液中加入几滴稀溴水没有白色沉淀出现 | 说明苯酚与溴没有发生反应 |
| C | 常温下白磷可自燃而氮气需要在放电时才与氧气反应 | 非金属性:P>N |
| D | 向相同体积、相同pH的两种一元酸中分别加入足量锌粉,测量产生氢气的体积 | 可以比较两种一元酸的酸性相对强弱 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| | 操作 | 预期现象及结论 |
| 方案1 | 取少量黄色溶液,加入NaOH溶液 | 如果生成红褐色沉淀,则说明发生了反应 |
| 方案2 | 取少量黄色溶液,加入淀粉碘化钾溶液 | 如果溶液变蓝色,则说明未发生反应 |
| 方案3 | 取少量黄色溶液,加入四氯化碳,振荡 | 如果下层溶液呈橙红色,则说明: |
| 实验操作 | 预期现象及结论 | 解释现象的离子方程式 |
| | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.皮肤上沾有少量苯酚,立即用大量浓氢氧化钠溶液洗去 |
| B.欲提纯鸡蛋白溶液中的蛋白质,用饱和的醋酸铅溶液进行盐析 |
| C.金属钠非常活泼,应将其保存在汽油中,以隔绝空气和水 |
D.仅 用溴水可鉴别苯、四氯化碳、2-戊烯、乙醇四种无色液体 用溴水可鉴别苯、四氯化碳、2-戊烯、乙醇四种无色液体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
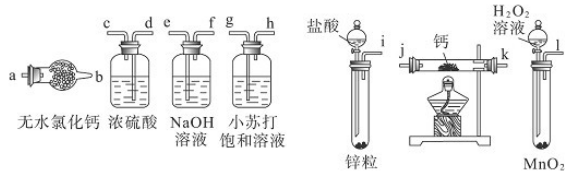
| A.加热反应一段时间 | B.收集气体并检验其纯度 |
| C.关闭分液漏斗活塞 | D.停止加热,充分冷却 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
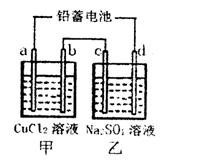
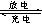 2PbSO4(s)+2H2O(1)。电解一段时间后,向c极和d极附近分别滴加酚酞试剂,c极附近溶液变红,下列说法正确的是______
2PbSO4(s)+2H2O(1)。电解一段时间后,向c极和d极附近分别滴加酚酞试剂,c极附近溶液变红,下列说法正确的是______ ______
______| A.d极为阴极 |
| B.若利用甲池精炼铜,b极应为粗铜 |
| C.放电时铅蓄电池负极的电极反应式为: PbO2(s)+4H+(aq)+ 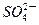 (aq)+4e- (aq)+4e- PbSO4(s)+2H2O(1) PbSO4(s)+2H2O(1) |
| D.若四个电极材料均为石墨,当析出6.4g Cu时,两池中共产生气体3.36L(标准 |
 H++A2-,请回答下列问题:
H++A2-,请回答下列问题: mol·L-1的NaHA溶液的pH=2,则0.1mol·L-1的H2A溶液中氢离子的物质的量浓度可能是__________0.1lmol·L-1(填“<”、“>”或“=”),理由是:___________________________.
mol·L-1的NaHA溶液的pH=2,则0.1mol·L-1的H2A溶液中氢离子的物质的量浓度可能是__________0.1lmol·L-1(填“<”、“>”或“=”),理由是:___________________________. CH3OH(g); △H=-90.8kJ·mol-1
CH3OH(g); △H=-90.8kJ·mol-1 CH3OH(g)
CH3OH(g) CH3OCH3(g)+H2O(g); △H=-23.5kJ·mol-1
CH3OCH3(g)+H2O(g); △H=-23.5kJ·mol-1 CO2(g)+H2(g);△=-41.3kJ·mol-1
CO2(g)+H2(g);△=-41.3kJ·mol-1 2SO3(g)。在一定温度下,将0.23 mol SO2和0.11 mol氧气放入容积为l L的密闭容器中发生反应,达到平衡后得到0.12 mol SO3,则反应的平衡常数K=________。若温度不变,再加入0.50 mol氧气后重新达到平衡,则SO3的体积分数将___________(填“增大”、“不变”或“减小”)。
2SO3(g)。在一定温度下,将0.23 mol SO2和0.11 mol氧气放入容积为l L的密闭容器中发生反应,达到平衡后得到0.12 mol SO3,则反应的平衡常数K=________。若温度不变,再加入0.50 mol氧气后重新达到平衡,则SO3的体积分数将___________(填“增大”、“不变”或“减小”)。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.NO(H2O含石蕊) | B.NH3(H2O含酚酞) | C.SO2 (NaOH溶液) | D.HCl(NaCl溶液) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com