
【题目】Ⅰ.欲配制0.18 mol·L-1醋酸钠溶液500 mL,可采用以下两种方案;
方案一:用托盘天平称取________g无水醋酸钠,溶于适量水中,配成500 mL溶液。定容时若仰视容量瓶刻度线,则所配制结果将___________(填“偏大”“偏小”或“无影响”)。
方案二:用体积均为250 mL且浓度均为________ mol·L-1的醋酸与氢氧化钠两溶液混合而成(设混合后的体积等于混合前两者体积之和)。
Ⅱ.某些非金属单质可以与强碱溶液发生反应。例如白磷(P4)可以与过量的热NaOH溶液反应生成PH3气体和NaH2PO2(次磷酸钠)。
(1)写出上述反应的化学方程式______________________________
(2) NaH2PO2 为__________ (填“正盐”或“酸式盐”),
(3)已知NaH2PO2水溶液pH>7,次磷酸的电离方程式为______________________;
NaH2PO2水溶液pH>7的原因:________________________________________。
(4)H3PO2 及 NaH2PO2均可将溶液中的 Ag+ 还原为银,从而可用于化学镀银。
利用(H3PO2)进行化学镀银反应中,氧化剂与还原剂的物质的量之比为 4︰1,则氧化产物为:
______________(填化学式)。
【答案】7.4偏小0.36P4 + 3NaOH + 3H2O === 3NaH2PO2 + PH3↑正盐H3PO2 ![]() H2PO2-+H+H2PO2-+H2O
H2PO2-+H+H2PO2-+H2O ![]() H3PO2+OH-H3PO4
H3PO2+OH-H3PO4
【解析】
Ⅰ.欲配制0.18 mol·L-1醋酸钠溶液500 mL,可采用以下两种方案;
方案一:根据n=c×V,m=n×M可知,用托盘天平称取无水醋酸钠质量为0.18×0.5×82= 7.4 g,定容时若仰视容量瓶刻度线,溶液的体积偏大,根据c=n/V可知,所配制结果将偏小;正确答案:7.4; 偏小。
方案二:醋酸和氢氧化钠1:1恰好完全反应生成醋酸钠,设醋酸浓度为cmol/L,0.25×c=0.18×0.5,c= 0.36 mol·L-1;正确答案:0.36。
Ⅱ.(1)根据电子守恒、原子守恒可知该反应的化学方程式:P4 + 3NaOH + 3H2O === 3NaH2PO2 + PH3↑;正确答案:P4 + 3NaOH + 3H2O === 3NaH2PO2 + PH3↑。
(2)根据题给信息可知,P4 与过量 的NaOH溶液反应生成NaH2PO2,因此,H3PO2为一元弱酸,所以NaH2PO2为正盐;正确答案:正盐。
(3)已知NaH2PO2水溶液pH>7,说明该盐属于强碱弱酸盐,次磷酸为一元弱酸,电离方程式为:H3PO2 ![]() H2PO2-+H+;H2PO2-水解,溶液显碱性,水溶液pH>7:H2PO2-+H2O
H2PO2-+H+;H2PO2-水解,溶液显碱性,水溶液pH>7:H2PO2-+H2O ![]() H3PO2+OH- ;正确答案:H3PO2
H3PO2+OH- ;正确答案:H3PO2 ![]() H2PO2-+H+ ;H2PO2-+H2O
H2PO2-+H+ ;H2PO2-+H2O ![]() H3PO2+OH-。
H3PO2+OH-。
(4) NaH2PO2为正盐,可将溶液中的Ag+ 还原为Ag,Ag元素的化合价降低,P元素的化合价升高,设氧化产物中P元素的化合价为x,由氧化剂与还原剂的物质的量之比为4:1及电子守恒可以知道: 4×(1-0)=1×(x-1),计算得出:x=+5;因此根据原子守恒规律可知氧化产物为H3PO4;正确答案:H3PO4。


科目:高中化学 来源: 题型:
【题目】在200 ℃时,将a mol H2(g)和b mol I2(g)充入到体积为V L的密闭器中,发生反应:I2(g)+H2(g)![]() 2HI(g)。
2HI(g)。
(1)反应刚开始时,由于c(H2)=______ mol·L-1,而c(HI)=________,所以化学反应速率________最大。(填v(正)或v(逆))。
(2)随着反应的进行,反应混合物中各组分浓度的变化趋势为c(H2)_____,而c(HI)_____ ,从而化学反应速率v(正) _______ (填减小、增大、不变)。
(3)当反应进行到v(正)与v(逆)________时,此可逆反应达到了最大限度。若保持外界条件不变时,混合物中各组分的物质的量、物质的量浓度、质量分数、体积分数、反应物的转化率和生成物的产率都将________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组设计了一组实验验证元素周期律。
Ⅰ.甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置来一次性完成元素氮、碳、硅非金属性强弱比较的实验研究。已知A是强酸,B是块状固体。打开分液漏斗的活塞后,可看到有大量气泡产生,烧杯中可观察到白色沉淀生成。
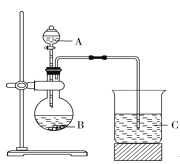
(1)甲同学设计实验的理论依据是_________________。
(2)写出选用的物质:A____________,B____________,C________(填化学式)。
(3)烧杯中反应的离子方程式为______________________。
(4)乙同学认为甲同学设计的实验不够严谨,应在B和C之间增加一个洗气装置,该装置中应盛放________(填试剂名称)溶液,目的是_____________________。
Ⅱ.丙同学设计了如图装置来验证卤族元素性质的递变规律。A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润的红纸。已知常温下浓盐酸与高锰酸钾能反应生成氯气。
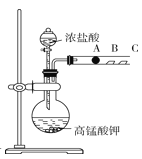
(5)A处的实验现象为_________;写出B处反应的离子方程式:____________;向NaBr和KI的混合溶液中,通入足量的Cl2充分反应后,将所得溶液蒸干并灼烧,最后得到的物质是_________。
(6)丙同学利用此实验证明卤素单质氧化性Cl2>Br2>I2,你认为此实验_____(填“合理”或“不合理”),理由是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】总的物质的量为0.50mol的Fe粉与Al粉混合物分为等质量的两份;在一份中加入足量的稀盐酸,在标准状况下产生气体aL;在另一份中加入足量的氢氧化钠溶液,在标准状况下产生气体bL。则a+b的数值不可能是( )
A. 5.6 B. 7.3 C. 8.2 D. 11.2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
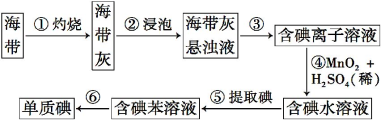
请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是_________(从下列仪器中选出所需的仪器,用标号字母填写空白处)。
A.烧杯
B.坩埚
C.表面皿
D.泥三角
E.酒精灯
F.干燥器
(2)步骤③的实验操作名称是 ;步骤⑥的目的是从含碘的苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是 。
(3)步骤④反应的离子方程式是 。
(4)步骤⑤中,某学生选择用苯来提取碘的理由是 。
(5)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.某探究小组在实验室中用铝土矿(主要成分为Al2O3,还含有Fe2O3、SiO2)提取氧化铝。回答下列问题:

(1)在实验中需用1 mol·L-1的NaOH溶液480 mL,配制该溶液已有下列仪器:烧杯、托盘天平(砝码)、胶头滴管、药匙、玻璃棒,还缺少的仪器是______________。
(2)写出步骤①中发生反应的离子方程式___________
(3)甲同学在实验室中用如图装置制备CO2气体,并通入滤液B中制备Al(OH)3时,结果没有产生预期现象。
乙同学分析认为:甲同学通入CO2的量不足是导致实验失败的原因之一,你认为乙的分析是否合理?________。若合理,请用离子方程式解释其原因_________________________________(若你认为不合理,该空不作答)。
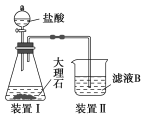
II.某实验小组为探究ClO-、I2、SO42-在酸性条件下的氧化性强弱,设计实验如下:
实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;
实验②:向实验①的溶液中加入4 mL 0.5 mol·L-1的亚硫酸钠溶液,蓝色恰好完全褪去。
(1)写出实验①中发生反应的离子方程式:_____________________________
(2)实验②的化学反应中转移电子的物质的量是_______________________。
(3)以上实验说明,在酸性条件下ClO-、I2、SO42-的氧化性由弱到强的顺序是__________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com