
下列氧化 还原反应中,1 mol H2O得到1 mol电子的是
还原反应中,1 mol H2O得到1 mol电子的是
A.Cl2+H2O===HCl+HClO
B.2Na2O2+2H2O===4NaOH+O2↑
C.2Na+2H2O===2NaOH+H2↑
D.3NO2+H2O===2HNO3+NO
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:
有4种碳骨架如下的烃,下列说法不正确的是( )
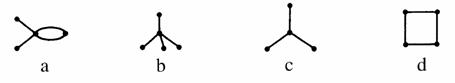
A.a和d互为同素异形体
B.b和c互为同系物
C.a和d都能发生加成反应
D.只有b和c能发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A. 物质发生化学反应都伴随着能量变化
B.伴有能量变化的物质变化都是化学变化
C.在一个确定的化学反应关系中,反应物的总能量总是高于生成物的总能量
D. 放热反应的发生无需任何条件
查看答案和解析>>
科目:高中化学 来源: 题型:
依据氧化还原反应: 2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:
(1)电极X的材料是______;电解质溶液Y是________;
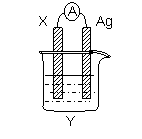 (2)银电极为电池的____极,发生的电极反应式为_______ ___;X电极上发生的电极反应为_____________________;(填反应类型)
(2)银电极为电池的____极,发生的电极反应式为_______ ___;X电极上发生的电极反应为_____________________;(填反应类型)
(3)外电路中的电子是从_______电极流向________电极。
(4)当有1.6g铜溶解时,银棒增重_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z为三种单质,已知:Y能将Z从其化合物的水溶液中置换出来,而Z又能将X从其化合物中置换出来。由此推断下列说法中可能正确的是
①单质的氧化性:Y>Z>X
②单质的还原性:Y>Z>X
③对应离子的氧化性:X>Z>Y
④对应离子的还原性:X>Z>Y
A.只有① B.只有②③
C.只有①④ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:①A+B2+===A2++B ②D+2H2O===D(OH)2+H2↑ ③以B、E为电极与E的盐溶液组成原电池,电极反应为:E2++2e-===E,B-2e-===B2+,下列说法正确的是
A.氧化性E2+>B2+>A2+>D2+
B.氧化性D2+>E2+>A2+>B2+
C.反应E+A2+===A+E2+能够进行
D.提取某废水中含有少量的A2+时可以选用D
查看答案和解析>>
科目:高中化学 来源: 题型:
仔细阅读下列三段文字:
①由稀有气体元素Xe(氙)与氧元素形成的一种共价化合物XeO3极不稳定,易转化为单质而呈强氧化性。将适量的XeO3投入含Mn2+的水溶液中,溶液逐渐变为紫红色且pH不断减小。
②将0.08 mol KMnO4固体(质量为12.64 g)加热一段时间后,收集到a mol O2;向反应后残留的固体中加入足量的浓盐酸,又收集到b mol Cl2,此时Mn元素全部以Mn2+的形式存在于溶液中。
③氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:
Cl2+2e-===2Cl-。
回答问题:
(1)试写出①有关的离子方程式:____________________________________________。
(2)请配平②的化学方程式:
________KMnO4+________HCl——________KCl+________MnCl2+________Cl2↑+________H2O
通过对第②段文字中提供的数据进行计算可得出:a+b的最大值为________,a+b最小值为________。
(3)下列四种物质中能使③中的还原过程发生的物质是________。
A.Na2CO3 B.KMnO4
C.XeO3  D.Na2SO3
D.Na2SO3
将该反应的氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并用单线桥表示电子转移的方向和数目:
 +
+
查看答案和解析>>
科目:高中化学 来源: 题型:
在室温下等体积的酸和碱的溶液,混合后pH一定小于7的是
( )
A.pH=3的硝酸和pH=11的氢氧化钾溶液
B.pH=3的盐酸和pH=11的氨水
C.pH=3的硫酸和pH=11的氢氧化钠溶液
D.pH=3的醋酸和pH=11的氢氧化钡溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
(1) )已知:C(s) + O2(g)  CO2(g) ΔH=-437.3 kJ•mol-1
CO2(g) ΔH=-437.3 kJ•mol-1
 H2(g) + O2(g)
H2(g) + O2(g)  H2O(g) ΔH=-285.8 kJ•mol-1
H2O(g) ΔH=-285.8 kJ•mol-1
CO(g) + O2(g)  CO2(g) ΔH=-283.0 kJ•mol-1
CO2(g) ΔH=-283.0 kJ•mol-1
则固态碳与水蒸汽反应生成一氧化碳和氢气的热化学方程式是
(2) 我国实施“嫦娥探月”行动的长征火箭中使用偏二甲肼[(CH3)2N—NH2]作为燃料,其与过氧化氢发生反应放出大量热量C2H8N2(l)+8H2O2(l)===N2(g)+2CO2(g)+12H2O(g) ΔH=-2 500 kJ/mol。如果1 mol偏二甲肼与过氧化氢发生上述反应生成液态水,则反应中放出的热量Q______2 500 kJ(填“<”、“>”或“=”)。
(3)恒温恒容下, 2 mol H2与2 mol N2反应达到平衡时,N2为1.8 mol,H2的转化率为________;若该反应在恒温恒压条件下进行(其他条件相同),反应达平衡时,H2的转化率比上述条件下H2的转化率________(填“大”、“小”或“相等”)。
(4)由甲烷、氧气和KOH溶液组成的新型燃料电池中,负极上发生反应的电极反应式为________________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com