
| 化学键 | Si-Si | O=O | Si-O |
| 键能/kJ·mol-1 | a | b | c |

 2NH3(g);△H<0,反应达到平衡后,测得混合气体为7体积。
2NH3(g);△H<0,反应达到平衡后,测得混合气体为7体积。
 SiO2(s) △H=(2a+ b - 4c)kJ/mol(2分)
SiO2(s) △H=(2a+ b - 4c)kJ/mol(2分) SiO2(s) △H=(2a+ b - 4c)kJ/mol。
SiO2(s) △H=(2a+ b - 4c)kJ/mol。

科目:高中化学 来源:不详 题型:单选题
| A.煤、石油和天然气都属于碳素燃料 |
| B.发展太阳能经济有助于减缓温室效应 |
| C.太阳能电池可将太阳能直接转化为电能 |
| D.目前研究菠菜蛋白质“发电”不属于“太阳能文明” |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2N2H4(g)+2NO2(g)=3N2(g)+4H2O(l);△H=-1135.7 kJ/mol |
| B.2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g);△H=-1000.3 kJ/mol |
| C.N2H4(g)+NO2(g)=3/2N2(g)+2H2O(l);△H=-1135.7 kJ/mol |
| D.2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g);△H=-1135.7 kJ/mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①② | B.①③ | C.②④ | D.③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.化学催化比酶催化的效果好 |
| B.使用不同催化剂可以改变反应的热效应 |
| C.使用不同催化剂可以改变反应的能耗 |
| D.反应物的总能量低于生成物的总能量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

A.NH3·H2O NH4++OH-达到平衡后,升高温度平衡正向移动 NH4++OH-达到平衡后,升高温度平衡正向移动 |
| B.在海轮的外壳上镶入锌块,可减缓船体的腐蚀速率 |
| C.明矾水解生成Al(OH)3胶体,可用作净水剂 |
| D.如图所示的反应过程中A+B→X的△H<0,X→C的△H>0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.S(s,单斜)=S(s,正交) ΔH=+0.33 kJ·mol-1 |
| B.正交硫比单斜硫稳定 |
| C.相同物质的量的正交硫比单斜硫所含有的能量高 |
| D.①式表示断裂1 mol O2中的共价键所吸收的能量比形成1 mol SO2中的共价键所放出的能量少297.16 kJ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.生成物总能量一定低于反应物总能量 |
| B.等量H2在O2中完全燃烧生成H2O(g)与生成H2O(l),放出的能量相同 |
| C.应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| D.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH不同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 P4O10。已知断裂下列化学键需要吸收的能量分别为:P—P a kJ·mol-1、P—O b kJ·mol-1、P
P4O10。已知断裂下列化学键需要吸收的能量分别为:P—P a kJ·mol-1、P—O b kJ·mol-1、P O c kJ·mol-1、O
O c kJ·mol-1、O O d kJ·mol-1。
O d kJ·mol-1。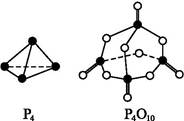
| A.(6a+5d-4c-12b) kJ·mol-1 |
| B.(4c+12b-6a-5d) kJ·mol-1 |
| C.(4c+12b-4a-5d) kJ·mol-1 |
| D.(4a+5d-4c-12b) kJ·mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com