
��14�֣���I�������й�ʵ��������У��������� ������ţ�
A����CCl4��ȡ��ˮ�еĵ⣬��Һʱ���л���ӷ�Һ©���¿ڷų�
B�������ô����������������ƻ�̼����
C����l0 g ZnSO4��7H2O�ܽ���90 gˮ������10����ZnSO4��Һ
D����ij��Һ�м��Ȼ�����Һ,����������ϡ����İ�ɫ����,�����Һ��һ������SO42��
E������һ�����ʵ���Ũ�ȵ���Һ������ʱ��������ƿ�Ŀ̶��ߣ���ʹ������ҺŨ��ƫ��
��II�����Ȼ���SCl2���۵㡪78�棬�е�59�档�ܶ�1.638g/mL����ˮ�ֽ⡣���Ȼ����������������ÿ�������Ҫ�����Լ��������ȣ�SOCl2��������������������Ӧ�ϳɶ��Ȼ����ʵ��װ�á�

�Իش����У�
��1��װ��A�з�Ӧ�����ӷ���ʽΪ�� ��
��2��װ��Bʢ�ŵ�ҩƷ�� ��C���� ��
��3��ʵ�鿪ʼǰ����D�з���һ��������ۣ�����ʹ���ۻ���Ȼ��ת����ҡ����ƿʹ��������ƿ�ڱ��γ�һ������棬��������Ŀ���� ��
��4��ʵ��ʱ��Dװ���������50��59 oC����ò��ú��ַ�ʽ ���ȡ�
��5��Fװ���и��������ʢ������ �������ǣ� ��
��6���ɶ��Ȼ�����SO3���������������ȵĻ�ѧ����ʽΪ�� ��
��I��A��B��E����II����1��MnO2+4H++2Cl-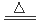 Mn2++Cl2��+2H2O��2�֣�
Mn2++Cl2��+2H2O��2�֣�
��2������ʳ��ˮ����ˮ����Ũ���ᣨ2�֣���3������Ӧ�Ӵ��� ��2�֣�
��4��ˮԡ���ȣ�����2�֣�����5����ʯ�ң�������������ƻ���ʯ�ң�����2�֣�
��ֹ������ˮ�������벢���ղ��������������2�֣�
��6�� SCl2 +SO3 = SOCl2 +SO2��2�֣�
��������
�����������I��A. ��CCl4��ȡ��ˮ�еĵ⣬����CCl4���ܶȱ�ˮ�����Է�Һʱ���л���ӷ�Һ©���¿ڷų�����ȷ��B. ���������ijɷ��ǹ����κ�SiO2���ڸ���ʱ�������ʻ�������κ�SiO2������Ӧ�����Բ����ô����������������ƻ�̼���ƣ���ȷ��C. ZnSO4��Һ��������ZnSO4����l0 g ZnSO4��7H2O�ܽ���90 gˮ������ZnSO4��Һ����������С��10��������D. ��ij��Һ�м��Ȼ�����Һ,����������ϡ����İ�ɫ����,�����Һ�п��ܺ���SO42����Ҳ���ܺ���Ag+������E.����һ�����ʵ���Ũ�ȵ���Һ������ʱ��������ƿ�Ŀ̶��ߣ�����Һ�������ƫС����ʹ������ҺŨ��ƫ�ߣ���ȷ����ѡ����A��B��E����II����1��װ��A����ʵ������ȡ������װ�á���Ӧ�����ӷ���ʽΪ��MnO2+4H++ 2Cl- Mn2++Cl2��+2H2O����2�����������лӷ��ԣ��������ȡ�������к�������HCl��H2O������װ��Bʢ�ŵ�ҩƷ�DZ���NaCl��Һ����ȥHCl����C����Ũ���ᣬ��ȥ���е�ˮ���ﵽ�ɾ����������������װ��D����S��Ӧ����SCl2����3��ʵ�鿪ʼǰ����D�з���һ��������ۣ�����ʹ���ۻ���Ȼ��ת����ҡ����ƿʹ��������ƿ�ڱ��γ�һ������棬��������Ŀ��������Ӧ�Ӵ��棬���Լӿ췴Ӧ���ʣ���4��ʵ��ʱ��Dװ���������50��59 oC��Ϊ�˸��õĿ��Ʒ�Ӧ�¶ȣ���ò��ú��ַ�ʽ��ˮԡ���ȣ���5������SCl2��ˮ�ֽ⣬Ϊ�˷�ֹSCl2ˮ�⣬������Fװ���и��������ʢ�����Ǹ������ʯ�ң�������������ƻ���ʯ�ң����������Ƿ�ֹ������ˮ�������벢���ղ��������������6�� �ɶ��Ȼ�����SO3���������������ȵĻ�ѧ����ʽΪSCl2 +SO3 = SOCl2 +SO2��
Mn2++Cl2��+2H2O����2�����������лӷ��ԣ��������ȡ�������к�������HCl��H2O������װ��Bʢ�ŵ�ҩƷ�DZ���NaCl��Һ����ȥHCl����C����Ũ���ᣬ��ȥ���е�ˮ���ﵽ�ɾ����������������װ��D����S��Ӧ����SCl2����3��ʵ�鿪ʼǰ����D�з���һ��������ۣ�����ʹ���ۻ���Ȼ��ת����ҡ����ƿʹ��������ƿ�ڱ��γ�һ������棬��������Ŀ��������Ӧ�Ӵ��棬���Լӿ췴Ӧ���ʣ���4��ʵ��ʱ��Dװ���������50��59 oC��Ϊ�˸��õĿ��Ʒ�Ӧ�¶ȣ���ò��ú��ַ�ʽ��ˮԡ���ȣ���5������SCl2��ˮ�ֽ⣬Ϊ�˷�ֹSCl2ˮ�⣬������Fװ���и��������ʢ�����Ǹ������ʯ�ң�������������ƻ���ʯ�ң����������Ƿ�ֹ������ˮ�������벢���ղ��������������6�� �ɶ��Ȼ�����SO3���������������ȵĻ�ѧ����ʽΪSCl2 +SO3 = SOCl2 +SO2��
���㣺�����������ȡ�����ӡ����ʵ�������Ŀ�ġ����ʵ�ʹ�á���ѧ����ʽ�����ӷ���ʽ����д��֪ʶ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�������ʡ�����и߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ������
��8�֣���һ��������ܱ������У��������»�ѧ��Ӧ��CO2(g)��H2(g)  CO(g)��H2O(g)���仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
CO(g)��H2O(g)���仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
t/�� | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
����������⣺
��1���÷�ӦΪ ������ȷ�Ӧ�������ȷ�Ӧ����
��2���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK��____________��
��3�����жϸ÷�Ӧ�Ƿ�ﵽ��ѧƽ��״̬��������________��
a��������ѹǿ���� b�����������c(CO)����
c��v��(H2)��v��(H2O) d��c(CO2)��c(CO)
��4��ij�¶��£�ƽ��Ũ�ȷ�����ʽ��c(CO2)��c(H2)��c(CO)��c(H2O)�����жϴ�ʱ���¶�Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ�߶���ѧ�����л�ѧ���ģ��Ծ��������棩 ���ͣ�ѡ����
����Ԫ���У�ԭ�Ӱ뾶��С����
A��Si B��P C��S D��Cl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ�߶���ѧ�����л�ѧ�������Ծ��������棩 ���ͣ�ѡ����
һ�������£�ij��Ӧ�Ļ�ѧ����ʽΪ��CO2��NO  NO2��CO ������˵����ȷ����
NO2��CO ������˵����ȷ����
A�������¶ȣ�����Ӧ���������淴Ӧ���ʼ���
B������ʱ��ѹ���������������ɫ�����ƽ������
C���ﵽƽ�⣬��ƽ�ⳣ��Ϊ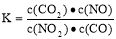
D������ʱ�������¶ȣ�����������ɫ����÷�Ӧ���ʱ�Ϊ��ֵ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ�߶���ѧ�����л�ѧ�������Ծ��������棩 ���ͣ�ѡ����
���淴Ӧ2HI(g) I2(g)+H2(g)���ܱ������н��У��������е������е�ij���ʱ��仯ʱ������˵����Ӧ�ﵽƽ�����
I2(g)+H2(g)���ܱ������н��У��������е������е�ij���ʱ��仯ʱ������˵����Ӧ�ﵽƽ�����
A������ֵ����ʵ��� B���������¶�
C��������ѹǿ D������������ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ������һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����֧�Թ��зֱ����������ͬ����ɫ��Һ�������²�����������ȷ����
���� | ���� | ���� | |
A | �μ�BaCl2��Һ | ���ɰ�ɫ���� | ԭ��Һ����SO42�� |
B | �μ���ˮ��CCl4�������� | �²���Һ����ɫ | ԭ��Һ����I�� |
C | �ýྻ��˿պȡ��Һ������ɫ��Ӧ | ����ʻ�ɫ | ԭ��Һ����Na+����K+ |
D | �μ�ϡNaOH��Һ����ʪ���ɫʯ����ֽ�����Թܿ� | ��ֽ������ | ԭ��Һ����NH4�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ������һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�ֱ��������������ӵ���Һ��ͨ�����������Ӳ�����ٵ���
A��HCO3- B��H+ C��Fe2+ D��Ag+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡ�����и�����ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
ij��Һ�п��ܺ���H+��NH4+��Mg2+��Al3+��Fe3+��CO32-��SO42-��NO3-�еļ��֡���������п����������ɫ��ζ�����壻��������NaOH��Һ��������ɫ�������Ҳ����ij����������NaOH�����ʵ���֮���
��ϵ��ͼ��ʾ��

������˵����ȷ����
A����Һ��һ������CO32-�����ܺ���SO42-��NO3-
B����Һ�е�������ֻ��H+��Mg2+��Al3+
C����Һ��n(NH4+)=0.2mol
D��n(H+)��n(Al3+)��n(Mg2+) = 1��1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ӱ�ʡ�����и���12��������ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й��������ʵ�Ӧ����ȷ����
A��Ũ��������ˮ�ԣ������ڸ��ﰱ���Ͷ�������
B����������ˮ���γɽ��壬����������ˮ��ɱ������
C�����������ܱ�Ũ����ۻ�������������������Ũ����
D�������ƾ���ǿ��ԭ�ԣ�������TiCl4��Һ��Ӧ��ȡ����Ti
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com