
工业上常用电解熔融氯化钠的方法制取金属钠和氯气,试回答下列问题:
(1) 金属钠在 阴 极上产生。
(2) 写出产生Cl2的电极反应方程式:
2Cl--2e- Cl2↑ 。
Cl2↑ 。
(3) 该反应 是 (填“是”或“不是”)离子反应。
科目:高中化学 来源: 题型:
按如图所示装置进行铁和水蒸气反应的实验。
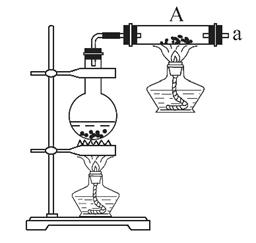
(1)铁粉与水蒸气反应的化学方程式是: ;
(2)为检验生成的气体产物,需从下图选择必要的装置,其正确的连接顺序为(用接口字母表示)a— ,描述能证明气体产物的实验现象_ ;

(3)停止反应,待装置冷却后,取出反应过的铁粉混合物,加入过量的稀硫酸充分反应。过滤。简述检验所得滤液中Fe3+的操作方法: ;
(4)经检验上述滤液中不含Fe3+,这不能说明铁粉与水蒸气反应所得产物中不含+3价的铁。原因是(用化学方程式说明): ;
(5)某同学利用上述滤液制取白色的Fe(OH)2沉淀,向滤液中加入NaOH溶液后,观察到生成的白色沉淀迅速变成灰绿色,最后变成红褐色。
①沉淀由白色变为红褐色的化学方程式是: ;
②为了得到白色的Fe(OH)2沉淀,并尽可能使沉淀长时间保持白色,有同学设计如下图所示的装置: 通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法中正确的是________(填序号)。
通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法中正确的是________(填序号)。
A.电源中的a为正极,b为负极 B.可以用NaCl溶液作为电解液
C.A、B两端都必须用铁作电极 D.阴极发生的反应是2H++2e-===H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
.化学与科学、技术、社会、环境密切相关。下列有关说法中错误的是
A.国庆节期间燃放的焰火的颜色是某些金属元素焰色反应所呈现出来的色彩
B.小苏打是制作馒头和面包等糕点的膨松剂,还是治疗胃酸过多的一种药剂
C.为防止中秋月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰或硅胶
D.青铜是我国使用最早的合金材料,目前世界上使用量最大的合金材料是钢铁
查看答案和解析>>
科目:高中化学 来源: 题型:
为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用含有铝、铁和铜的合金废料制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾晶体。
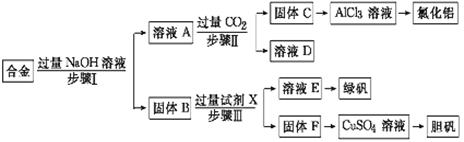
请回答:
(1)写出步骤Ⅰ反应的离子方程式: 。
(2)试剂X是 。步骤Ⅰ、Ⅱ、Ⅲ中均需进行的实验操作是 。
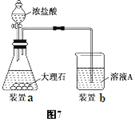
(3)进行步骤Ⅱ时,该小组用如图7所示装置及试剂制取CO2并将制得的气体通入溶液A中。一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为了避免固体C减少,可采取的改进措施是 。
(4)用固体F制备CuSO4溶液,可设计以下三种途径:

写出途径①中反应的离子方程式 ,请选出你认为的最佳途径并说明选择的理由 。
查看答案和解析>>
科目:高中化学 来源: 题型:
氯的原子序数为17,37Cl和35Cl是氯的两种同位素,下列说法正确的是 ( )
A.35Cl所含质子数为18
B. mol的H35Cl分子所含中子数约为6.02×1023
mol的H35Cl分子所含中子数约为6.02×1023
C.3.5 g的35Cl2气体的体积为2.24 L
D.35Cl2气体的摩尔质量为70 g·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
英国《卫报》最近评出了“人类最糟糕的发明”,我们使用的塑料袋不幸获得这一殊荣,这是因为它对生态环境造成了严重污染,为了防治污染,有一条重要的途径是将合成高分子化合物重新变成小分子化合物,目前对结构简式为:
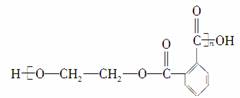 的物质已经成功地实现了这种处理,试分析若用CH3OH来处理它,能得到的有机物可能是( )
的物质已经成功地实现了这种处理,试分析若用CH3OH来处理它,能得到的有机物可能是( )
① 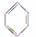 ②HOCH2CH2OH
②HOCH2CH2OH
③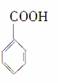 ④
④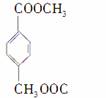
A.①④ B.②④ C.②③ D.①③
查看答案和解析>>
科目:高中化学 来源: 题型:
由于吸水、透气性较好,高分子化合物“维纶”常用于生产内衣、桌布、窗帘等,其结构简式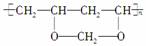 ,它是由聚乙烯醇(
,它是由聚乙烯醇(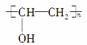 )与另一单体经缩合反应得到的。若已知缩合过程中有H2O生成,则与聚乙烯醇缩合的单体可能是( )
)与另一单体经缩合反应得到的。若已知缩合过程中有H2O生成,则与聚乙烯醇缩合的单体可能是( )
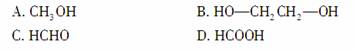
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下在密闭容器中加入NH4I发生反应:
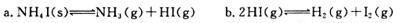
则反应a的平衡常数表达式为___________;达到平衡后,扩大容器体积,反应b的移动方向______________(填正向、逆向或不移动)
(2)氮元素的+4价氧化物有两种,它们之间发生反应:2NO2 N2O4 △H < 0,将一定量的NO2充入注射器中后封口,下图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是_____________
N2O4 △H < 0,将一定量的NO2充入注射器中后封口,下图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是_____________
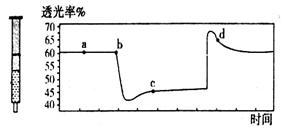
A.b点的操作是压缩注射器 B.c点与a点相比,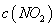 增大,
增大,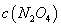 减小
减小
C.若反应在一绝热容器中进行,则b、c两点的平衡常数Kb>Kc
 D.d点:
D.d点: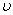 (正)>
(正)>  (逆)
(逆)
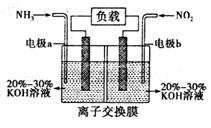
(3)利用反应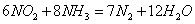 构成原电池,能消除氮氧化物的排放,减轻环境污染,装置如图所示。
构成原电池,能消除氮氧化物的排放,减轻环境污染,装置如图所示。
①电极a为______极,其电极反应式为________________
②当有2.24 L NO2(标准状况下)被处理时,转移电子为____________mol
③为使电池持续放电,该离子交换膜需选用_______(选填“阳”或“阴”)离子交换膜。
 (4)使用硼氢化钠(NaBH4)为诱导剂,可使Co2+与肼(N2H4)在碱性条件下发生反应,制得高纯度纳米钴,该过程不产生有毒气体。
(4)使用硼氢化钠(NaBH4)为诱导剂,可使Co2+与肼(N2H4)在碱性条件下发生反应,制得高纯度纳米钴,该过程不产生有毒气体。
①写出该反应的离子方程式______________________________。
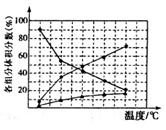
②在纳米钴的催化作用下,肼(N2H4)可分解生成两种气体,其中一种气体能使湿润的红色石蕊试纸变蓝。若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如图所示,为抑制肼的分解,可采取的合理措施有_______________________________________________ (任写一种)。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知氨基酸可发生如下反应: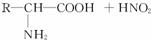
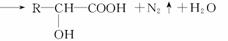
且已知:D、E的相对分子质量分别为162和144,可发生如下物质转化关系,如下图所示:
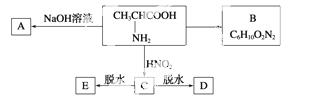
(1)写出B、D的结构简式:B____________,D_______________。
(2)写出C→E的化学方程式:__________________________________________。
(3)写出C→D的化学方程式:________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com