

科目:高中化学 来源:不详 题型:单选题
| A.HX和CH3COOH均可抑制水的电离 |
| B.取HCl与HX各0.1 mol溶于水配制成1 L混合溶液,则溶液的c(H+)=0.2 mol·L-1 |
| C.等物质的量浓度、等体积的HX溶液与CH3COONa溶液混合后所得的溶液中:c(Na+)>c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) |
| D.向等物质的量浓度、等体积的HX溶液和CH3COOH溶液中,分别加入一定物质的量浓度的NaOH溶液,欲使两者的pH均等于7,则消耗氢氧化钠溶液的体积:前者大于后者 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 HR + HS-, 2Z-+ H2S(少量)
HR + HS-, 2Z-+ H2S(少量) 2HZ + S2-。下列叙述正确的是
2HZ + S2-。下列叙述正确的是| A.相同温度下电离平衡常数:Ki1(H2S)>Ki(HZ)>Ki2(H2S)>Ki(HR) |
| B.结合H+的能力:Z->S 2->R->HS- |
| C.同温同浓度下,溶液的pH值:NaHS>NaR>Na2S>NaZ |
D.HZ与Na2S反应的离子方程式:HZ +S2- HS- + Z- HS- + Z- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.取等体积的醋酸和盐酸,分别稀释至原溶液的m倍和n倍,结果两溶液的pH仍然相同,则m<n |
| B.取等体积的两种酸分别与完全一样的足量锌粒反应,开始时反应速率:盐酸大于醋酸 |
| C.取等体积的两种酸,分别用完全一样的NaOH溶液进行中和,醋酸消耗NaOH的物质的量比盐酸消耗的多 |
| D.两种酸中c (CH3COO-) > c (Cl-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
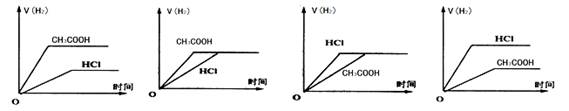
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用HNO2溶液作导电试验,灯光较暗 |
| B.HNO2是共价化合物 |
| C.亚硝酸不与氯化钠反应 |
| D.常温下0.1 mol?L-1亚硝酸溶液的c(H+)为7.1×10-3 mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 酸 | 电离常数(25oC) |
| 碳酸 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
| 次溴酸 | Ki=2.4×10-9 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A. ×100% ×100% | B. ×100% ×100% |
C. ×100% ×100% | D. ×100% ×100% |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.相同浓度的两溶液中c(H+)相同 |
| B.100mL0.1mol/L的两溶液能中和等物质的量的氢氧化钠 |
| C.pH=3的两溶液都稀释10倍,盐酸的pH大于醋酸的PH |
| D.两溶液中分别加人少量对应的钠盐,c(H+)均明显减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com