
反应2SO2+O22SO3经一段时间后,SO3的浓度增加了0.4 mol·L-1,在这段时间内用O2表示的反
应速率为0.04 mol·L-1·s-1,则这段时间为 ( )
A.0.1 s B.2.5 s C.5 s D.10 s
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:
某温度下在容积为 2L 的密闭容器中,发生反应 2X(g) + Y(g) 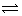 2W(g);△H<0,当充入 2 mol X 和 1 mol Y,经20 s达到平衡时生成了 0.4 molW。下列说法正确的是()
2W(g);△H<0,当充入 2 mol X 和 1 mol Y,经20 s达到平衡时生成了 0.4 molW。下列说法正确的是()
①升高温度,W 的体积分数减小,△H 增大
②以 Y 的浓度变化表示的反应速率为 0.01 mol/(L·s)
③在其它条件不变的情况下,增加 1 mol X ,则 X 和 Y 的转化率均提高
④增大压强,正反应速率增大,逆反应速率减小,则平衡向正反应方向移动
⑤再向容器中通入 2 mol X 和 1 mol Y,达到平衡时,X、Y 的转化率均增大。
A、①⑤ B、⑤ C、②③④ D、④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
pH=13的NaOH溶液与pH=2的H2SO4溶液混合,所得溶液的pH=11,则NaOH溶液与H2SO4溶液的体积比是( ).
A.11∶1 B.9∶1 C.1∶11 D.1∶9.
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨N2+3H2 2NH3的反应速率可以分别用v(H2)、v(N2)、v(NH3)(单位为mol·L-1·s-1)表示,则下
2NH3的反应速率可以分别用v(H2)、v(N2)、v(NH3)(单位为mol·L-1·s-1)表示,则下
列表示正确的是( )
A.v(H2)=v(N2)=v(NH3) B.v(H2)=v(N2)
C.v(NH3)=3/2v(H2) D.v(H2)=3v(N2)
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B两种 气体在一定条件发生反应:
气体在一定条件发生反应:
aA(g)+bB(g)cC(g)+dD(g)
取a mol A和b mol B置于容积为V L的容器内,1 min后,测得容器中A的浓度为x mol·L-1。则此时B的浓度为________,C的浓度为________,以A的浓度变化表示的反应速率为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在一密闭容器中发生反应N2+3H22NH3,达到平衡后,只改变某一个条件时,反应速率与反应时间
的关系如图所示:
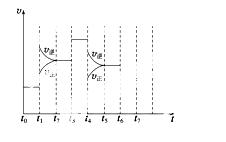
回答下列问题:
(1)处于平衡状态的时间段是________(填选项)。
A.t0~t1 B.t1~t2 C.t2~t3
D.t3~t4 E.t4~t5 F.t5~t6
(2)t1、t3、t4时刻分别改变的一个条件是(填选项)。
A.增大压强 B.减小压强 C.升高温度
D.降低温度 E.加催化剂 F.充入氮气
t1时刻________;t3时刻________;t4时刻________。
(3)依据(2)中的结论,下列时间段中,氨的百分含量最高的是__________(填选项)。
A.t0~t1 B.t2~t3
C.t3~t4 D.t5~t6
(4)如果在t6时刻,从反应体系中分离出部分氨,t7时刻反应达到平衡状态,请在图中画出反应速率的变化曲线。
(5)一定条件下,合成氨反应达到平衡时,测得混合气体中氨气的体积分数为20%,则反应后与反应前的混合气体体积之比为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
2SO2(g)+O2(g)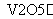 2SO3(g)是制备硫酸的重要反应。下列叙述正确的是( )
2SO3(g)是制备硫酸的重要反应。下列叙述正确的是( )
A.催化剂V2O5不改变该反应的逆反应速率
B.增大反应体系的压强,反应速率一定增大
C.该反应是放热反应,降低温度将缩短反应达到平衡的时间
D.在t1、t2时刻,SO3(g)的浓度分别是c1、c2,则时间间隔t1~t2内,SO3(g)生成的平均反应速率为v=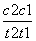
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)某化学兴趣小组对“农夫山泉”矿泉水进行检测时,发现1.0 L该矿泉水中含有45.6 mg Mg2+,则该矿泉水中Mg2+的物质的量浓度为 。
(2)在KCl和CaCl2所组成的某混合物中,K+与Ca2+的物质的量之比为2∶1,则KCl与CaCl2的物质的量之比为 ,该混合物中CaCl2的质量分数为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A、B、C为中学化学中常见的单质.室温下,A为固体,B和C均为气体.在适宜的条件下,它们可以按下图进行反应.
回答下列问题:
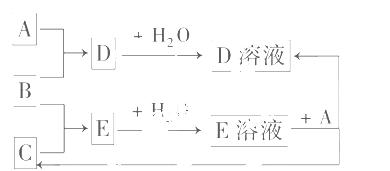
(1)A、B、C三种元素中的任意两种元素形成的化合物所属物质类别一定不是 .
①氢化物 ②酸 ③碱 ④盐 ⑤氧化物
(2)A、B、C三种元素中有一种是金属,则这种元素是A、B、C中的 ,理由是 .
(3)如果E溶液是一种强酸,则E的化学式为  .
.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com