
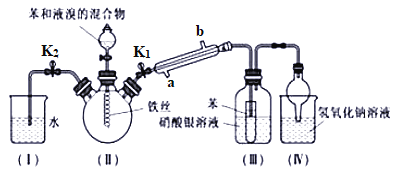
【题目】某校学生用下图所示装置进行实验。以探究苯与溴发生反应的原理并分离提纯反应的产物。
请回答下列问题:
(1)写出装置Ⅱ中发生的主要化学反应方程式____________________________,其中冷凝管所起的作用为导气和________,Ⅳ中球形干燥管的作用是__________。
(2)实验开始时,关闭K2、开启K1和分液漏斗活塞,滴加苯和液溴的混合液,反应开始。Ⅲ中小试管内苯的作用是_________________________。
(3)能说明苯与液溴发生了取代反应的现象是______________________。
(4)反应结束后,要让装置Ⅰ中的水倒吸入装置Ⅱ中以除去装置Ⅱ中残余的HBr气体。简述如何实现这一操作:______________________________________。
(5)纯净的溴苯是无色油状的液体,这个装置制得的溴苯呈红棕色,原因是里面混有______________,将三颈烧瓶内反应后的液体依次进行下列实验操作就可得到较纯净的溴苯。①用蒸馏水洗涤,振荡,分液;②用__________洗涤,振荡,分液;③蒸馏。
【答案】 ![]() 冷凝回流(冷凝苯和Br2蒸气) 防倒吸 吸收溴蒸气 III中硝酸银溶液内出现淡黄色沉淀 关闭K1和分液漏斗活塞,开启K2 溴(Br2) NaOH溶液
冷凝回流(冷凝苯和Br2蒸气) 防倒吸 吸收溴蒸气 III中硝酸银溶液内出现淡黄色沉淀 关闭K1和分液漏斗活塞,开启K2 溴(Br2) NaOH溶液
【解析】苯和液溴发生取代反应生成溴苯和溴化氢,由于液溴易挥发,会干扰溴化氢的检验,需要利用苯除去溴。利用氢氧化钠溶液吸收尾气,由于溴化氢极易溶于水,需要有防倒吸装置,根据生成的溴苯中含有未反应的溴选择分离提纯的方法。据此解答。
(1)装置Ⅱ中发生的主要化学反应是苯和液溴的取代反应,反应的化学方程式为![]() 。由于苯和液溴易挥发,则其中冷凝管所起的作用为导气和冷凝回流(冷凝苯和Br2蒸气)。由于溴化氢极易溶于水,则Ⅳ中球形干燥管的作用是防倒吸。
。由于苯和液溴易挥发,则其中冷凝管所起的作用为导气和冷凝回流(冷凝苯和Br2蒸气)。由于溴化氢极易溶于水,则Ⅳ中球形干燥管的作用是防倒吸。
(2)Ⅲ中小试管内苯的作用是除去溴化氢中的溴蒸气,避免干扰溴离子检验;
(3)因从冷凝管出来的气体为溴化氢,溴化氢不溶于苯,溴化氢能与硝酸银反应生成溴化银沉淀,因此能说明苯与液溴发生了取代反应的现象是III中硝酸银溶液内出现淡黄色沉淀。
(4)因装置Ⅱ中含有溴化氢气体能污染空气,使I的水倒吸入Ⅱ中可以除去溴化氢气体,以免逸出污染空气;操作方法为关闭K1和分液漏斗活塞,开启K2。
(5)纯净的溴苯是无色油状的液体,这个装置制得的溴苯呈红棕色,原因是里面混有单质溴,由于单质溴能与氢氧化钠溶液反应,则将三颈烧瓶内反应后的液体依次进行下列实验操作就可得到较纯净的溴苯。①用蒸馏水洗涤,振荡,分液;②用氢氧化钠溶液洗涤,振荡,分液;③蒸馏。


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】用如下图所示装置可以完成一系列实验(图中夹持装置已略去)

请回答下列问题:
Ⅰ. 若气体a是Cl2,装置A、B、C中的试剂依次为: FeCl2溶液、淀粉KI溶液、石蕊溶液。
(1)A溶液由浅绿色变为棕黄色,反应的离子方程式为_________________________________。
(2)B瓶中的淀粉KI溶液变为蓝色,反应的离子方程式为______________________________。
(3)C瓶中的现象为_______________________________________________________________。
(4)D装置中试剂为_______________________________________________________________。
II.若气体a是SO2,装置A、B、C中的试剂依次为:品红溶液、酸性高锰酸钾溶液、氢硫酸(硫化氢的水溶液)。
(1)A瓶中品红和B瓶中酸性高锰酸钾溶液均褪色,其中体现了SO2漂白性的是 _____(填写序号A或B)。
(2)C瓶中产生淡黄色沉淀, 反应的化学方程式_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.
Ⅰ.配制0.50mol/L NaOH溶液
(1)若实验中大约要使用245mL NaOH溶液,至少需要称量NaOH固体g.
(2)从图中选择称量NaOH固体所需要的仪器是(填字母): .
名称 | 托盘天平(带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
仪器 |
|
|
|
|
|
|
序号 | a | b | c | d | e | f |
(3)Ⅱ.测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示.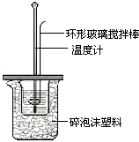
写出该反应的热化学方程式(中和热为57.3kJ/mol): .
(4)取50mL NaOH溶液和30mL硫酸溶液进行实验,实验数据如下表.
①请填写下表中的空白:
温度 | 起始温度t1/℃ | 终止温度 | 温度差平均值 | ||
H2SO4 | NaOH | 平均值 | |||
① | 26.2 | 26.0 | 26.1 | 30.1 | |
② | 27.0 | 27.4 | 27.2 | 33.3 | |
③ | 25.9 | 25.9 | 25.9 | 29.8 | |
④ | 26.4 | 26.2 | 26.3 | 30.4 | |
②近似认为0.50mol/L NaOH溶液和0.50mol/L硫酸溶液的密度都是1g/cm3 , 中和后生成溶液的比热容c=4.18J/(g℃).则中和热△H=(取小数点后一位).
③上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是(填字母) .
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由1﹣溴丁烷制取少量的1,2﹣丁二醇 ![]() 时,需要经过下列哪几步反应( )
时,需要经过下列哪几步反应( )
A.取代、消去、加成
B.加成、消去、取代
C.消去、加成、取代
D.消去、加成、消去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是( )
A.乙烯与苯都能使溴水褪色,但褪色原理不同
B.1 mol乙烯与Cl2完全加成,然后与Cl2发生取代反应,共消耗氯气5mol
C.溴水遇到乙醛溶液出现褪色现象,是因为它们发生了氧化反应
D.二氯甲烷存在两种不同的结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着原子序数的递增,下列说法正确的是( )
A.最外层电子数逐渐增多
B.原子半径逐渐减小
C.元素的主要化合价逐渐增加
D.元素的化合价、原子半径、最外层电子数、得失电子能力、金属性与非金属性呈周期性变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,下列药物的主要成分都能发生四种反应的是( )
①取代反应 ②加成反应③水解反应 ④中和.
A.维生素B5: 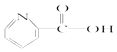
B.阿司匹林: 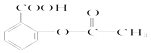
C.芬必得: 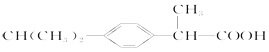
D.摇头丸: 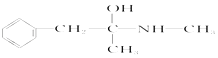
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,改变0.1mol/L RCOOH溶液的pH,溶液中RCOOH、RCOO-的微粒分布分数a(X)= ![]() ;甲酸(HCOOH)与丙酸(CH3CH2COOH)中酸分子的分布分数与PH的关系如图所示。
;甲酸(HCOOH)与丙酸(CH3CH2COOH)中酸分子的分布分数与PH的关系如图所示。
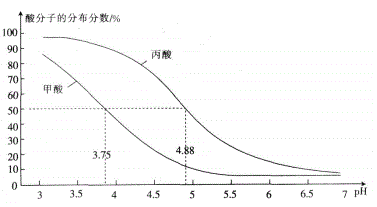
下列说法正确的是
A. 丙酸的酸性比甲酸强
B. 若0.1mol/L甲酸溶液的pH= 2.33,则0.01mol/L甲酸溶液的pH= 3.33
C. CH3CH2COOH![]() CH3CH2COO-+H+的lgK=-4.88
CH3CH2COO-+H+的lgK=-4.88
D. 将0.1mol/L的HCOOH溶液与0.lmol/L的HCOONa溶液等体积混合,所得溶液中:c(Na+)>c(HCOOH)>c(HCOO-)>c(OH-)>c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com