
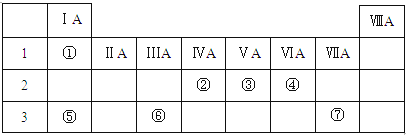
���� ����Ԫ�������ڱ��е�λ��֪���٢ڢۢܢݢޢ߷ֱ���H��C��N��O��Na��Al��ClԪ�أ�
��1���γɵľ�����������ṹ�ķ���ֻ�м��飻
��2��ͬ����Ԫ�ش�����Ԫ�صķǽ���������ǿ��
��3��Ԫ�آܵĵ��ʺ�Ԫ�آݵĵ����ڿ�����ȼ������Na2O2��
��4��Ư�۵���Ч�ɷ�ΪCa��ClO��2��
��5��Ԫ�آݵ�����������Ӧ��ˮ������Ԫ�آĵ��ʷ�����Ӧ����ƫ�����ƺ�������
��6��������γɵĻ�����ΪNH3��ʵ�������������ƺ��Ȼ���ڼ����������Ʊ�Ԫ�آ���ۡ�Ԫ�آ�����γɵĻ�����ֱ�ΪNH3��HCl������������ˮ���������������ֱ�պȡ���ǵ�Ũ��Һ����ӽ�ʱ�����Ȼ�泥�
��� �⣺����Ԫ�������ڱ��е�λ��֪���٢ڢۢܢݢޢ߷ֱ���H��C��N��O��Na��Al��ClԪ�أ�
��1��7��Ԫ������Ԫ�آ��γɵľ�����������ṹ�ķ���ֻ�м�����ϣ��ʴ�Ϊ�����飻
��2��ͬ����Ԫ�ش�����Ԫ�صķǽ���������ǿ���ʴ�Ϊ����ǿ��
��3��Ԫ�آܵĵ��ʺ�Ԫ�آݵĵ����ڿ�����ȼ������Na2O2������ʽΪ2Na+O2$\frac{\underline{\;��ȼ\;}}{\;}$Na2O2���ʴ�Ϊ��2Na+O2$\frac{\underline{\;��ȼ\;}}{\;}$Na2O2��
��4��Ư�۵���Ч�ɷ�ΪCa��ClO��2���ʴ�Ϊ��Ca��ClO��2��
��5��Ԫ�آݵ�����������Ӧ��ˮ������Ԫ�آĵ��ʷ�����Ӧ����ƫ�����ƺ���������Ӧ�����ӷ���ʽΪ2Al+2OH-+2H2O=2AlO2-+3H2����
�ʴ�Ϊ��2Al+2OH-+2H2O=2AlO2-+3H2����
��6��������γɵĻ�����ΪNH3��ʵ�������������ƺ��Ȼ���ڼ����������Ʊ�����Ӧ�Ļ�ѧ����ʽΪCa��OH��2+2NH4Cl$\frac{\underline{\;\;��\;\;}}{\;}$CaCl2+2NH3��+2H2O��
Ԫ�آ���ۡ�Ԫ�آ�����γɵĻ�����ֱ�ΪNH3��HCl������������ˮ���������������ֱ�պȡ���ǵ�Ũ��Һ����ӽ�ʱ�����Ȼ�泥��ɿ������������а������ɣ�
�ʴ�Ϊ��Ca��OH��2+2NH4Cl$\frac{\underline{\;\;��\;\;}}{\;}$CaCl2+2NH3��+2H2O�����ɰ��̣�
���� ���⿼����Ԫ�����ڱ���Ԫ�������ɵ��ۺ�Ӧ�ã�Ϊ�߿��������ͣ��漰ԭ�ӽṹ���������Ԫ�������ɵ�֪ʶ�㣬��ȷԭ�ӽṹ���������Ԫ����������������ɣ���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������Ȼ������Ҫ�ɷ֣�����������京̼��Ϊ75% | |
| B�� | �Ҵ��ķ���ʽΪC2H6O����������һ����ɫҺ�壬�ܶȱ�ˮС | |
| C�� | ����Ľṹ��ʽ��CH3COOH���ܺ�ˮ������Ȼ��ܣ����Ա�̼��ǿ | |
| D�� | ��ϩ����Ҫ�Ļ���ԭ�ϣ���ʹ��ˮ�����Ը��������Һ��ɫ������Ư������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
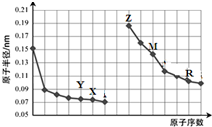
| A�� | �����ӵİ뾶��С�Ƚϣ�Y��X��Z | |
| B�� | ��̬�⻯���ȶ��ԣ�X��R | |
| C�� | R����������Ӧˮ�����м������Ӽ����й��ۼ� | |
| D�� | Z�����ܴ�M������Һ���û�������M |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 20mL 0.5mol/L AlCl3��Һ | B�� | 30mL 1mol/L KCl��Һ | ||
| C�� | 7.5mL 2mol/L MgCl2��Һ | D�� | 10mL 3mol/L NaCl��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��2L�ܱ���������X��Y��Z�������������·����Ŀ��淴Ӧ�����ǵ����ʵ�����ʱ��仯���仯��������ͼ��ʾ�����з�����ȷ���ǣ�������
��2L�ܱ���������X��Y��Z�������������·����Ŀ��淴Ӧ�����ǵ����ʵ�����ʱ��仯���仯��������ͼ��ʾ�����з�����ȷ���ǣ�������| A�� | 4 min�� v��Z��=0.025 mol•L-1•min-1 | |
| B�� | Y��ƽ��ת����Ϊ75% | |
| C�� | ƽ�ⳣ��K=��25/12����mol•L-1��-2 | |
| D�� | t1 minʱ��������He��ƽ���������ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
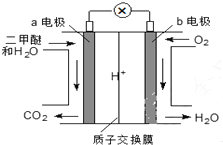 �����ѣ�CH3OCH3����һ����ɫ��������������Դ����ͼ����ɫ��Դ��ȼ�ϵ�ء��Ĺ���ԭ��ʾ��ͼ��a��b��Ϊ���Pt�缫�����õ�ع���ʱ������˵������ȷ���ǣ�������
�����ѣ�CH3OCH3����һ����ɫ��������������Դ����ͼ����ɫ��Դ��ȼ�ϵ�ء��Ĺ���ԭ��ʾ��ͼ��a��b��Ϊ���Pt�缫�����õ�ع���ʱ������˵������ȷ���ǣ�������| A�� | a�缫Ϊ�õ�ظ��� | |
| B�� | O2��b�缫�Ϸ�ӦΪO2+2H2O+4e-=4OH- | |
| C�� | ��ع���ʱ����a�缫����1molCH3OCH3�ŵ磬��·����12mol����ת�� | |
| D�� | ��ع���ʱ������ڲ�H+��a�缫����b�缫 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com