


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡģ���� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��ɽ��ʡģ���� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
![]() ˮ������֮Դ��2005��12�·�������ʡ�ı���ˮ��Ⱦ�¼��ٴ��������DZ���ˮ��Դ�ı�Ҫ�Ժͽ����ԡ�
ˮ������֮Դ��2005��12�·�������ʡ�ı���ˮ��Ⱦ�¼��ٴ��������DZ���ˮ��Դ�ı�Ҫ�Ժͽ����ԡ�
![]() (1)�ݱ���������ˮ��Ⱦ�¼�������ijұ�����豸�����ڼ��ŷŵķ�ˮ���£��Ʋ�����Ҫ��Ⱦ���� ������к���ˮ�Ѿ��ں�������ɢ��Ϊ�˾�������Σ�����Ժ�ˮ�Ĵ���Ӧ�ò�ȡ�Ĵ�ʩ��
(1)�ݱ���������ˮ��Ⱦ�¼�������ijұ�����豸�����ڼ��ŷŵķ�ˮ���£��Ʋ�����Ҫ��Ⱦ���� ������к���ˮ�Ѿ��ں�������ɢ��Ϊ�˾�������Σ�����Ժ�ˮ�Ĵ���Ӧ�ò�ȡ�Ĵ�ʩ��
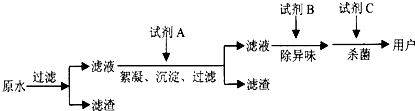
![]() (2)����ˮ������������ͼ�����е��Լ�A��B��C�ֱ����ѡ�� �� �� ��
(2)����ˮ������������ͼ�����е��Լ�A��B��C�ֱ����ѡ�� �� �� ��
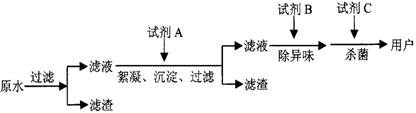
(3)��Ƴ��ŷŵķ�ˮ�к���(��Cr2O72����ʽ����)�����õ��ķ������������ʱ������Ϊ���������ɵ�Fe2+��Cr2O72����ԭΪCr3+������������ʱ���ɵ�OH-�γ����������������ȥ��
�������缫�Ϸ����ķ�Ӧ�ֱ�Ϊ������ ������ ��
����Һ�з������ܷ�ӦΪ(�����ӷ���ʽ��ʾ) ��
(4)��ѧ������(COD)��ˮ�������Ŀ�����Ŀ��һ����������ˮ�л�ԭ����Ⱦ�����Ҫָ�ꡣCOD��ָ��ǿ������(�ҹ�����K2Cr2O7)����һ����ˮ��ʱ���ĵ�����������,���������O2��Ϊ������ʱ,1Lˮ��������O2������(mg?L-1)����ȡij����ˮ��20.00mL,��Ӧ����10.00mL0.0400mol?L-1K2Cr2O7��Һ(��Ӧ��ת��ΪCr3+)����ˮ����CODΪ mg?L-1��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com