

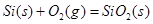 ;
;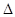 H="-989.2"
H="-989.2" 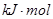
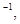 则x的值为 ( )
则x的值为 ( ) | A.460 | B.920 | C.1 165.2 | D.423.3 |
 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:高中化学 来源:不详 题型:单选题
| A.NaOH:固 | B.盐酸:液 | C.NaCl:溶液 | D.H2O:溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 化学反应 | 平衡常数 | 温度(℃) | |
| 500 | 800 | ||
①2H2(g)+CO(g) CH3OH(g) CH3OH(g) | K1 | 2.5 | 0.15 |
②H2(g)+CO2(g) H2O (g)+CO(g) H2O (g)+CO(g) | K2 | 1.0 | 2.50 |
③3H2(g)+ CO2(g) CH3OH(g)+H2O (g) CH3OH(g)+H2O (g) | K3 | | |


查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.194 | B.391 | C.516 | D.658 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
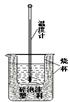
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氯化钠 | B.固体硝酸铵 | C.固体氢氧化钠 | D.生石灰 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.①② | B.②③ | C.③④ | D.②④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.生成物总能量一定低于反应物总能量 |
B.同温同压下,H2(g)+Cl2(g)=2HCl(g) 在光照和点燃条件下的 H不同 H不同 |
C.一定条件下,0.5 mol N2和1.5 mol H2置于某密闭容器中充分反应生成NH3气,放热19.3 kJ,其热化学方程式为N2(g)+3H2(g) 2NH3(g) 2NH3(g)  H =-38.6 kJ/mol H =-38.6 kJ/mol |
| D.一定条件下4 HCl(g)+O2(g)=2Cl2(g)+2H2O(g) ,当1 mol |

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.化合反应都大多是放热反应 |
| B.凡是需要加热的反应,都是吸热反应 |
| C.体系的混乱度增大的反应都是吸热反应 |
| D.中和反应是放热反应,其化学能可以转化成电能 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com