
| A. | X、Y两端都必须用铁作电极 | B. | 不可以用NaOH溶液作为电解液 | ||
| C. | 阴极发生的反应是:2H++2e-=H2↑ | D. | 白色沉淀只能在阳极上产生 |
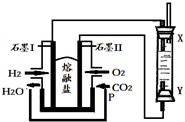
分析 左边装置是原电池,为氢氧燃料电池,通入氢气的电极I为负极、通入氧气的电极II为正极,负极反应式为H2-2e-+CO32-═CO2+H2O,正极反应式为O2+4e-+2CO2=2CO32-,右边装置是电解池,X是阴极、Y是阳极,阴极反应式为2H2O+2e-=H2↑+2OH-、阳极反应式为Fe-2e-+2OH-=Fe(OH)2↓,则Y电极材料应该为Fe,据此分析解答.
解答 解:左边装置是原电池,为氢氧燃料电池,通入氢气的电极I为负极、通入氧气的电极II为正极,负极反应式为H2-2e-+CO32-═CO2+H2O,正极反应式为O2+4e-+2CO2=2CO32-,右边装置是电解池,X是阴极、Y是阳极,阴极反应式为2H2O+2e-=H2↑+2OH-、阳极反应式为Fe-2e-+2OH-=Fe(OH)2↓,则Y电极材料应该为Fe,
A.通过以上分析知,Y电极必须是Fe,但X电极不一定是Fe,故A错误;
B.电解过程是阴极上H+放电生成氢气,同时生成OH-,OH-和Fe2+反应生成Fe(OH)2,溶液呈碱性,所以可以用NaOH溶液作为电解液,故B错误;
C.阴极上H+放电生成氢气,阴极反应式为2H++2e-=H2↑,故C正确;
D.电解时电解质溶液中阳离子向阴极移动,所以白色沉淀可以在阴极产生,故D错误;
故选C.
点评 本题考查电解原理及化学电源新型电池,为高频考点,注意把握原电池的工作原理以及电极反应式的书写,解答本题的关键是根据物质的性质判断原电池的正负极,难点是燃料电池电极反应式的书写.


科目:高中化学 来源: 题型:选择题
| A. | 150 mL 1 mol/L盐酸 | B. | 20 mL 18.4 mol/L硫酸 | ||
| C. | 50 mL 3 mol/L盐酸 | D. | 250 mL 2 mol/L硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO是一种红棕色气体 | |
| B. | NO2与水反应生成硝酸,所以NO2是硝酸的酸酐 | |
| C. | NO和NO2是引发光化学烟雾的主要污染源 | |
| D. | NO2可用排水法收集 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
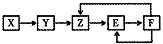 五种常见物质X、Y、Z、E、F均含有同一元素M,已知Y是单质,Z是NO(一氧化氮),在一定条件下它们有如下转化关系,下列推断不合理的是( )
五种常见物质X、Y、Z、E、F均含有同一元素M,已知Y是单质,Z是NO(一氧化氮),在一定条件下它们有如下转化关系,下列推断不合理的是( )| A. | X可能是一种氢化物 | B. | M不可能是金属 | ||
| C. | E可能是一种有色气体 | D. | X→Y一定是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
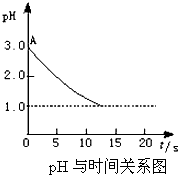 某课题小组的同学对“电解氯化铜溶液时的pH变化”的问题,有以下两种不同的观点:
某课题小组的同学对“电解氯化铜溶液时的pH变化”的问题,有以下两种不同的观点:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 油脂皂化生成的高级脂肪酸钠是肥皂的有效成分 | |
| B. | 重金属盐能使蛋白质变性,所以误食重金属盐会中毒 | |
| C. | 在入海口的钢铁闸门上装一定数量的铜块可防止闸门被腐蚀 | |
| D. | 禁止使用四乙基铅作汽油抗爆震剂,可减少汽车尾气污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=0的溶液中:Fe3+、Mg2+、Cl-、SO42- | |
| B. | 水电离出的c(H+)=1×10-13mol/L的溶液中:K+、HCO3-、Cl-、S2- | |
| C. | 甲基橙呈红色的溶液中:Fe3+、Na+、SO42-、CO32- | |
| D. | 在AlCl3溶液中:Na+、AlO2-、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com