
���������Ȼ�ѧ����ʽ�У��йء�H�ıȽ���ȷ���ǣ� ��
��CH4(g)+O2(g)=CO2(g)+2H2O(g) ��H1
CH4(g)+2O2(g)=CO2(g)+2H2O(1) ��H2
��NaOH(aq)+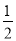 H2SO4��Ũ��=
H2SO4��Ũ��=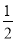 Na2SO4(aq)+H2O(1) ��H3
Na2SO4(aq)+H2O(1) ��H3
NaOH (aq)+CH3 COOH( aq)=CH3COONa( aq)+H2O(1) ��H4
A����Hl>��H2����H3>��H4, B����HI>��H2����H3<��H4
C����H1=��H2����H3 =��H4 D����Hl<��H2����H3<��H4

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ¦���е���У�߶������л�ѧ���������棩 ���ͣ�ѡ����
����˵����ȷ����( )
A�������£�PH=9��̼������Һ����ˮ�������c(OH��)=1��10-9mol��L-1
B��������ˮ�У� c(Cl��)=c(ClO��)��c(HClO)
C����pH��4�Ĵ�����Һϡ�ͺ���Һ���������ӵ�Ũ�Ⱦ�����
D���к͵����pH��ͬ��H2SO4��HCl��Һ������NaOH�����ʵ���Ϊ2:1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���������������ʡ��У��һ��ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ʵ����
���ڻ����ķ�����ᴿ�������õķ����У��ٹ��ˡ�����������������ȡ���ݼ��ȷֽ�ȡ����и������ķ�����ᴿӦ����ʲô������������ţ�
��1����ȡ��ˮ�еĵ�____________��
��2����ȥʳ����Һ�е�ˮ____________��
��3��������ˮ____________��
��4����ȥKC1�����к��е�����KC1O3____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���������������ʡ��У�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ʵ����
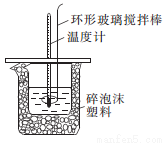
��1��������������������___________________��
��2���кͷ�Ӧ�ų���������������������ڷ�Ӧ�лӷ������õ��к��ȵ���ֵ________���ƫ����ƫС�����䡱����
��3����ʵ��С����������ʵ�飬ÿ��ȡ��Һ��50 mL������ʵ�����ݼ�¼���£�
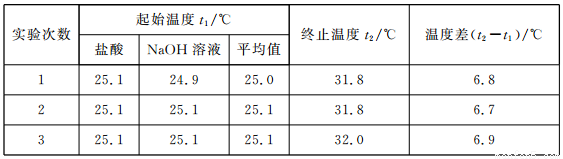
��֪���ᡢNaOH��Һ���ܶ���ˮ��ͬ���кͺ����ɵ���Һ�ı�����c=4��18��10-3kJ��(g����)����÷�Ӧ���к��ȡ�H=__________��
��4�����к��Ȳⶨʵ���У�������ʼ�¶�ʱ��Ҫ�����¶ȼƣ����ֻ��һ���¶ȼƲ��������õ��к��ȵ���ֵ___________���ƫ����ƫС�����䡱����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���������������ʡ��У�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
�뵼�幤ҵ��ʯӢɰ��ԭ��ͨ������������Ҫ��Ӧ�������ʹ裺

��ʯӢɰ����1.00 kg���裬�ų���������ԼΪ�� ��
A��2.43��104KJ B��2��35��104 kJ C��2��23��104 kJ D��2��14��104 kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���������������ʡ��У�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��̪��ϡ��ˮ�м�������NH4 Cl���壬��Һ��ɫ�� ��
A������ɫ B������ C����dz D������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�긣��ʡ��һ�����л�ѧ���������棩 ���ͣ�ѡ����
���в�������Һ�ĵ��������仯�������
A��Ba(OH)2��Һ�е���H2SO4��Һ������ B���������еμӰ�ˮ
C������ʯ��ˮ��ͨ��CO2��ǡ����ȫ���� D��NH4Cl��Һ������NaOH����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�긣��ʡ��һ�����л�ѧ���������棩 ���ͣ�ѡ����
����˵���в���ȷ���ǣ� ��
����ͬһ��Ԫ����ɵ������ǵ���
��������һ����������Ԫ�أ�������һ��������Ԫ��
�۽���������һ���Ǽ���������
�ܼ���������һ���ǽ���������
�ݷǽ���������һ��������������
������������һ���Ƿǽ���������
�����Ԫ����һ������������е�Hԭ����
A���٢ڢܢݢ� B���٢ۢݢ� C���٢ڢۢݢ� D���ۢܢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ������ʮ��У�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ������
�������ֳ����£�N2H4����ɫҺ�壩��һ��Ӧ�ù㷺�Ļ���ԭ�ϣ����������ȼ�ϣ��ش��������⣺
��1���������ӵĵ���ʽΪ_____________�����е��Ļ��ϼ�Ϊ_____________��
��2��ʵ���ҿ��ô���������Һ�백��Ӧ�Ʊ���������Ӧ�����ӷ���ʽΪ____________________��
��3����2O2(g)+N2(g)=N2O4(l) ��H1
��N2(g)+2H2(g)=N2H4(l) ��H2
��O2(g)+2H2(g)=2H2O(g) ��H3
��2N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) ��H4
������Ӧ��ЧӦ֮��Ĺ�ϵʽΪ��H4=_______________���á�H1����H2����H3��ʾ����
��4������Ϊ��Ԫ�����ˮ�еĵ��뷽��ʽ�백���ƣ�������һ�����뷴 Ӧ��ƽ�ⳣ��ֵΪ
Ӧ��ƽ�ⳣ��ֵΪ
(��֪��N2H4 + H+  N2H5+ K=8.5��
N2H5+ K=8.5�� 107��Kw=1.0��10-14)�������������γɵ���ʽ�εĻ�ѧʽΪ ��
107��Kw=1.0��10-14)�������������γɵ���ʽ�εĻ�ѧʽΪ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com