
| 0.05mol |
| 1mol/L |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
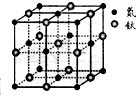 现有5种短周期元素A、B、C、D、E,原子序数依次增大.A的同位素中有一种核素无中子,B最外层上电子数是次外层电子数的两倍,C元素最简单的氢化物Y的水溶液呈碱性,E是短周期中电负性最小的元素.D与可与A、B、C、E四种元素分别形成原子个数比不相同的常见化合物.回答下列问题:
现有5种短周期元素A、B、C、D、E,原子序数依次增大.A的同位素中有一种核素无中子,B最外层上电子数是次外层电子数的两倍,C元素最简单的氢化物Y的水溶液呈碱性,E是短周期中电负性最小的元素.D与可与A、B、C、E四种元素分别形成原子个数比不相同的常见化合物.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 某反应2A(g)?2B(g)+C(g)(吸热反应)在2L密闭容器中的三种不同条件下进行,B、C的起始浓度为0,A的浓度(mol/L)随反应时间(min)的变化情况如图所示
某反应2A(g)?2B(g)+C(g)(吸热反应)在2L密闭容器中的三种不同条件下进行,B、C的起始浓度为0,A的浓度(mol/L)随反应时间(min)的变化情况如图所示查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在离子化合物中不可能存在非极性键 |
| B、气体单质分子中一定存在非极性键 |
| C、在共价化合物中不可能存在离子键 |
| D、由非金属元素组成的化合物一定是共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 △H=+88.62kJ/mol
△H=+88.62kJ/mol| A、一定条件下,1mol NBD最多可与2 mol Br2发生加成反应 |
| B、物质Q的能量比NBD的低 |
| C、物质Q的一氯取代物只有3种 |
| D、NBD和Q二者互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、煤燃烧是化学能转化为热能的过程 |
| B、化石燃料和植物燃料燃烧时放出的能量均来源于太阳能 |
| C、动物体内葡萄糖被氧化成CO2是化学能转变成热能的过程 |
| D、植物通过光合作用将CO2转化为葡萄糖是太阳能转变成热能的过程 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com