
根据下面的反应路线及所给信息填空。

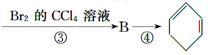
(1)A的结构简式是__________,名称是__________。
(2)①的反应类型是________;③的反应类型是__________________________。
(3)反应④的化学 方程式是____________。
方程式是____________。
科目:高中化学 来源: 题型:
过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。关于双氧水,回答下列问题:
A.N a2O2 + 2HCl ==== 2NaCl + H2O2 B.Ag2O + H2O2 ==== 2Ag + O2↑ + H2O
a2O2 + 2HCl ==== 2NaCl + H2O2 B.Ag2O + H2O2 ==== 2Ag + O2↑ + H2O
C.2H2O2 ==== 2H2O + O2↑ D.3H2O2 + Cr2(SO4)3 + 10KOH ==== 2K2CrO4 + 3K2SO4 + 8H2O
(1)上述反应中,不属于氧化还原反应是__________。(填字母序号,下同)
(2)保存过氧化氢的试剂瓶上最适合贴上的一个标签是__________。
(3)某强酸性反应体系中,反应物和生成物共六种物 质或离子:O2、MnO4-、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2↑。
质或离子:O2、MnO4-、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2↑。
①该反应的离子方程式是__________ 。
②如果上述反应中有2.24L(标准状况)气体生成,转移的电子的物 质的量为__________mol。
质的量为__________mol。
(4)H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称;如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:KCN + H2O2 + H2O ==== A + NH3↑,试指出生成物A的化学式为__________,并阐明H2O2被称为“绿色氧化剂”的理由是_______________。
(5)请设计一个简单易行的实验证明过氧化氢具有氧化性。除过氧化氢外,供选择的试剂还有:氯水、稀硝酸、饱和硫化氢溶液。请将所选试剂和实验现象填入下表:
| 实验内容 | 试剂 | 实验现象 |
| 验证氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
乙醇、甘油和苯酚的共同点是( )
A.分子结构中都含有羟 基,都能与Na反应,产生H2
基,都能与Na反应,产生H2
B.都能与NaOH溶液发生中和反应
C.与FeCl3溶液反应呈紫色
D.常温下都是无色液体
查看答案和解析>>
科目:高中化学 来源: 题型:
合成P(一种抗氧剂)的路线如下:

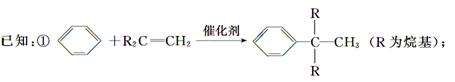
②A和F互为同分异构体,A分子中有三个甲基,F分子中只有一个甲基。
(1)A—→B的反应类型为________。B经催化加氢生成G(C4H10),G的化学名称是________。
(2)A与浓HBr溶液一起共热生成H,H的结构简式为______________。
(3)实验室中检验C可选择下列试剂中的________。
a.盐酸 b.FeCl3溶液
c.NaHCO3溶液 d.浓溴水
(4)P与足量NaOH溶液反应的化学反应方程式为__________________(有机物用结构简式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
胡妥油(D)用作香料的原料,它可由A合成得到:
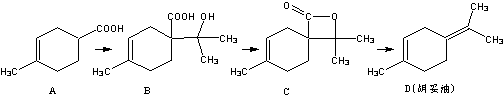
下列说法正确的是
A.若有机物A是由异戊二烯(C5H8)和丙烯酸(C3H4O2)加热得到的,则该反应的反应类型属于加成反应
B.有机物D分子中所有碳原子一定共面
C.有机物C 的所有同分异构体中不可有芳香族化合物存在
D.有机 物B 既能跟Na反应放出H2,又能跟NaHCO3溶液反应放出CO2气体
物B 既能跟Na反应放出H2,又能跟NaHCO3溶液反应放出CO2气体
查看答案和解析>>
科目:高中化学 来源: 题型:
归纳与推理是化学学习常用的方法。下列推理正确的是
A.因为稀硫酸能与铁反应放出H2,所以稀硝酸与铁反应也一定能放出H2
B.因为Na可以与水反应放出H2,所以K也可以与水反应放出H2
C.因为CO2的水溶液可以导电,所以CO2是电解质
D.因为SO2可以使酸性KMnO4溶液褪色,所以SO2具有漂白性
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液与Al反应能放出H2,下列离子在该溶液中一定能大量共存的是
A.NH4+、Fe2+、NO3-、SO42- B.Na+、K+、Cl-、SO42-
C.Mg2+、H+、Cl-、NO3- D.K+、Ca2+、HCO3-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
|
| A. | 常温常压下,23g的NO2含有的氧原子数为NA |
|
| B. | 已知某种元素的一种原子的质量为ag,则该元素的相对原子质量近似为aNA |
|
| C. | 某密闭容器盛有0.1molN2和0.4molH2,在一定条件下充分反应,转移电子的数目为0.6NA |
|
| D. | 80gNH4NO3晶体中含有NH4+小于NA个 |
查看答案和解析>>
科目:高中化学 来源: 题型:
为验证氧化性:Cl2>Fe3+>SO2,某
小组用下图所示装置进行实验(夹持仪器和甲中加热装置已略,气密性已检验)。
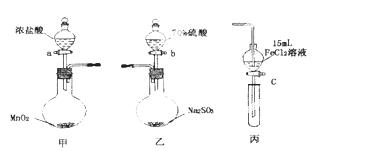
实验步骤:
①在甲装置中,打开活塞a,加热,待装置中充满黄绿色气体时,与丙装置连接。
②当丙装置中FeC12溶液变黄时,停止加热。
③打开活塞c,使约2mL的溶液滴入试管中,检验溶液中的离子。
④在乙装置中,打开活塞b,待空气排尽后,将乙中产生的气体通入上述丙装置变黄后的溶液中,一段时间后停止。
⑤更新丙中试管,打开活塞c,使约2mL的溶液滴入试管中,检验溶液中的离子。
回答下列问题:
(1)甲中发生反应的化学方程式为___________________________________________。
(2)用70%的硫酸制取SO2,反应速率比用98%的硫酸快,原因是__________________。
(3)实验中,证明氧化性Fe3+>SO2的离子方程式为_____________________________。
(4)有I、II、III三组同学分别完成了上述实验,实验结果如下:
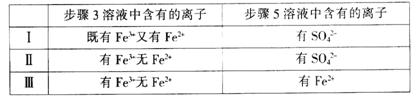
上述实验结果一定能够证明氧化性:Cl2>Fe3+>SO2的是___________(用“I”、“II”、“III”代号回答)。
(5)若要用以上甲和丙装置证明氧化性为:Cl2> Fe3+> I2的结论,则步骤为:
①往丙的漏斗中加入两种试剂_________、_________和一种溶剂__________。
②将甲装置中产生的Cl2慢慢通入丙中,观察丙的漏斗中溶液颜色变化。
③如果观察到丙中溶液_______________________________________则结论正确。
④停止通入Cl2。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com