
分析 (1)根据盖斯定律由已知的热化学方程式乘以相应的数值进行加减,来构造目标热化学方程式,反应热也乘以相应的数值进行加减;
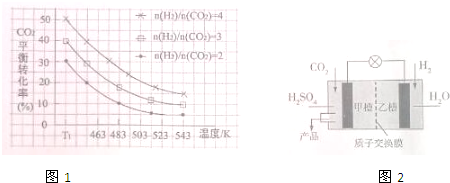
(2)①根据图1可知,温度为T1K时,在1L反应容器中投入2molCO2和8molH2进行反应即n(H2)/n(CO2)比值=4时,达平衡时CO2的转化率为50%,据此计算;
②根据图1,当n(H2)/n(CO2)比值固定时,随着温度升高,达平衡时CO2的转化率在减小;作一与横坐标垂直的等温线,可以看出其他条件不变,达平衡时CO2的转化率随n(H2)/n(CO2)比值增大而增大;
(3)随原料气中n(CO)/{n(CO)+n(CO2)}比值的增大,即CO的含量增大,反应③平衡将向逆方向移动,既消耗大量的水,又增大了CO2和氢气的含量,从而促使反应①向正反应方向移动,这又增大了CH3OH的含量,又促使②的平衡向正向移动,则二甲醚产率增大,据此分析;
(4)根据图2,甲槽为CO2得电子发生还原反应生成CH3OH,据此书写反应式.
解答 解:(1)已知反应:①CO2(g)+3H2(g )?CH3OH(g)+H2O(g)△H1=-49.1 kJ•mol-1
②2CH3OH(g)?CH3OCH3(g)+H2O(g)△H2=-24.5 kJ•mol-1
根据盖斯定律:①×2+②即得到目标方程式,所以CO2(g)加H2(g)转化为CH3OCH3(g) 和H2O(g)的热化学方程式2CO2(g)+6H2(g)?CH3OCH3 (g)+3H2O(g)△H=(-49.1×2-24.5)kJ•mol-1=-122.7 kJ•mol-1,
故答案为:2CO2(g)+6H2(g )?CH3OCH3 (g)+3H2O(g)△H=-122.7 kJ•mol-1;
(2)①由图1可知,温度为T1K时,在1L反应容器中投入2molCO2和8molH2进行反应即n(H2)/n(CO2)比值=4时,达平衡时CO2的转化率为50%,所以平衡时CO2的浓度为$\frac{2mol×(1-50%)}{1L}$=1mol/L,故答案为:1mol/L;
②根据图1,当n(H2)/n(CO2)比值固定时,随着温度升高,达平衡时CO2的转化率在减小;作一与横坐标垂直的等温线,可以看出其他条件不变,达平衡时CO2的转化率随n(H2)/n(CO2)比值增大而增大;故答案为:其他条件不变,达平衡时CO2的转化率随温度升高而减小;其他条件不变,达平衡时CO2的转化率随n(H2)/n(CO2)比值增大而增大;
(3)随原料气中n(CO)/{n(CO)+n(CO2)}比值的增大,即CO的含量增大,反应③平衡将向逆方向移动,既消耗大量的水,又增大了CO2和氢气的含量,从而促使反应①向正反应方向移动,这又增大了CH3OH的含量,又促使②的平衡向正向移动,则二甲醚产率增大,故答案为:随着CO的含量增大,反应③平衡将向逆方向移动,既消耗大量的水,又增大了CO2和氢气的含量,从而促使反应①和②的平衡都向正向移动,则二甲醚产率增大;
(4)根据图2,甲槽为CO2得电子发生还原反应生成CH3OH,反应式为CO2+6e-+6H+═CH3OH+H2O,故答案为:CO2+6e-+6H+═CH3OH+H2O.
点评 本题考查的知识点较多,题目综合性较强,难度较大,主要考查了盖斯定律的应用、化学平衡的有关计算、图表信息的提取与应用等,在书写电池的电极方程式时要注意电解质对反应的影响.


 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案科目:高中化学 来源: 题型:选择题
| A. | 元素B、C、D的原子半径由大到小的顺序为:r(D)>r(C)>r(B) | |
| B. | C的单质在点燃条件分别与A、B、D的单质化合,所得化合物均存在共价键 | |
| C. | 四种元素的单质中,熔沸点最高的是D的单质 | |
| D. | C和D所形成离子的电子层结构一定相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
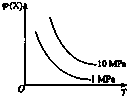
| A. | 2NH3(g)?N2(g)+3H2(g)(正反应为吸热反应) | |
| B. | H2(g)+I2(g)?2HI(g)(正反应为放热反应) | |
| C. | 4NH3(g)+5O2(g)?4NO(g)+6H2O(g)(正反应为放热反应) | |
| D. | 2SO2(g)+O2(g)?2SO3(正反应为放热反应) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图为甲、乙两种物质的溶解度曲线图,请根据图回答下列问题.
如图为甲、乙两种物质的溶解度曲线图,请根据图回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 甲烷、甲醇、CO、H2、CO2均是重要的化工原料.
甲烷、甲醇、CO、H2、CO2均是重要的化工原料.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某有机物燃烧只生成CO2和H2O,且二者物质的量相等,则有机物的组成为一定CnH2n | |
| B. | 相同物质的量的烃,完全燃烧,生成的CO2越多,说明烃中的碳的百分含量越大 | |
| C. | 气态烃CxHy在O2充分燃烧,反应前后气体体积不变(温度>100℃),则y=4 | |
| D. | 相同质量的烃,完全燃烧,消耗O2越多,烃中碳的百分含量越高 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度,正向反应速率增加,逆向反应速率减小 | |
| B. | 升高温度有利于反应速率增加,从而缩短达到平衡的时间 | |
| C. | 若反应在密闭体系内进行,通入He气,体系压强增大,反应速率增大 | |
| D. | 若反应在恒压体系内进行,通往He气,体系压强不变,反应速率不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com