
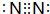 .
.分析 X、Y、Z、W是短周期元素中的四种非金属,它们的原子序数依次增大,X元素的原子形成的离子就是一个质子,则X为H元素;Y原子的最外层电子数是内层电子数的2倍,原子只能有2个电子层,最外层电子数为4,故Y为C元素;Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体,则Z为N元素、W为O元素,据此解答.
解答 解:X、Y、Z、W是短周期元素中的四种非金属,它们的原子序数依次增大,X元素的原子形成的离子就是一个质子,则X为H元素;Y原子的最外层电子数是内层电子数的2倍,原子只能有2个电子层,最外层电子数为4,故Y为C元素;Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体,则Z为N元素、W为O元素.
(1)Z单质为N2,分子中氮原子之间形成3对共用电子对,电子式为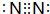 ,故答案为:
,故答案为: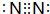 ;
;
(2)氢气和氮气在一定条件下反应生成化合物E为NH3,氨气与CuO反应生成生成Cu、氮气与水,该反应的化学方程式为:2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O,
故答案为:2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O;
(3)由H、N、O三种元素组成的一种速效肥料盐是NH4NO3,含有离子键、共价键;
H、C、N、O四种元素可组成酸式盐为NH4HCO3,与足量NaOH溶液在加热条件下反应生成碳酸钠、氨气与水,反应离子方程式为:NH4++HCO3-+2OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+2H2O+CO32-,
故答案为:NH4NO3;离子键、共价键;NH4++HCO3-+2OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+2H2O+CO32-;
(4)工业上用氨气检验输送氯气的管道是否漏气,可观察到大量白烟,同时有单质氮气生成,生成的白烟为氯化铵,化学方程式为:8NH3+3Cl2=6NH4Cl+N2;该反应中氯气为氧化剂,氨气为还原剂,8mol氨气反应,只有2mol被氧化,被氧化的氨气与参与反应的氨气的质量之比2mol:8mol=1:4,
故答案为:8NH3+3Cl2=6NH4Cl+N2;1:4.
点评 本题考查位置结构与性质关系的综合应用,正确推断各元素为解答关键,试题知识点较多、综合性较强,充分考查学生对知识的迁移运用,难度中等.


 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案科目:高中化学 来源: 题型:选择题
| A. | CH3CHO→C2H5OH | B. | C2H5OH→CH2=CH2 | ||
| C. | 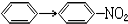 | D. | CH3COOH→CH3COOC2H5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl-离子的结构示意图: | B. | 白磷分子的比例模型: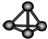 | ||
| C. | H2O2的结构式:H-O-O-H | D. | CCl4的电子式: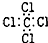 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol•L-1醋酸,溶液的pH=1 | |
| B. | 0.1mol•L-1醋酸加水稀释,溶液中离子浓度都减小 | |
| C. | 0.1mol•L-1氨水溶液中:c(OH-)=c(NH${\;}_{4}^{+}$) | |
| D. | 0.1mol•L-1氨水与0.1mol•L-1 HCl溶液等体积混合所得溶液中:c(Cl-)>c(NH${\;}_{4}^{+}$)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 与HCN反应引入:
与HCN反应引入: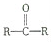 $→_{一定条件}^{HCN}$
$→_{一定条件}^{HCN}$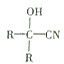
 $→_{一定条件①}^{HCN}$ A $→_{②}^{H_{2}O,H+}$ B$→_{③}^{浓H_{2}SO_{4},△}$ C $→_{催化剂④}^{聚合}$ D
$→_{一定条件①}^{HCN}$ A $→_{②}^{H_{2}O,H+}$ B$→_{③}^{浓H_{2}SO_{4},△}$ C $→_{催化剂④}^{聚合}$ D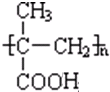 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 工业上和净化后的水煤气在催化剂作用下,与水蒸气发生反应制取氢气,化学方程式为:CO(g)+H2O(g)?H2(g)+CO2(g).一定条件下,将4molCO与2molH2O(g)充入体积为2L的密闭容器中,体系中各物质的深度随时间变化如图所示:
工业上和净化后的水煤气在催化剂作用下,与水蒸气发生反应制取氢气,化学方程式为:CO(g)+H2O(g)?H2(g)+CO2(g).一定条件下,将4molCO与2molH2O(g)充入体积为2L的密闭容器中,体系中各物质的深度随时间变化如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl晶体中阴、阳离子 | B. | NH3分子中的质子和电子 | ||
| C. | Na2O2固体中阴、阳离子 | D. | ${\;}_{1}^{2}$H原子中的质子和中子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Li在空气中的燃烧产物为Li2O2 | B. | Be(OH)2 溶于NaOH可生成BeO2- | ||
| C. | BeO是两性氧化物 | D. | B2O3既能溶于强酸又能溶于强碱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com