
分析 物质导电有两种原因,一是有自由移动的电子能够导电,二是能够产生自由离子的溶液能够导电;
电解质:在水溶液中或熔融状态下能够导电的化合物;
非电解质:在熔融状态和水溶液中都不能导电的化合物.
解答 解:①NaCl固体不能导电,在水溶液中能导电,是电解质;
②液态SO3不能导电,且自身不能电离,是非电解质;
③液态的醋酸不能导电,在水溶液中能够导电,是电解质;
④汞为金属单质,存在自由移动的电子,能导电,既不是电解质也不是非电解质;
⑤BaSO4固体不能导电,在水溶液中或熔融状态下能够导电,是电解质;
⑥纯蔗糖(C12H22O11)不能导电,是非电解质;
⑦酒精(C2H5OH)不能电离属于非电解质;
⑧熔化的KNO3能导电,是电解质;
(1)能导电的是④⑧;
故答案为:④⑧;
(2)属于电解质的是 ①③⑤⑧;
故答案为:①③⑤⑧;
(3)属于非电解质的是 ②⑥;
故答案为:②⑥⑦.
点评 本题考查物质的导电性的判断,电解质、非电解质概念的辨析,题目难度不大.解题时紧抓住电解质必须是化合物,以及导电是在水溶液或熔化状态下为条件.


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案科目:高中化学 来源: 题型:选择题
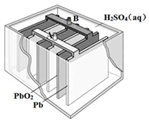 铅蓄电池是最常见的二次电池,其构造示意图如下.发生反应的化学方程式为:
铅蓄电池是最常见的二次电池,其构造示意图如下.发生反应的化学方程式为:| A. | 放电时,电解质溶液的PH值增大 | |
| B. | 放电时,电路中转移0.2mol电子时Pb电极质量减少20.7g | |
| C. | 放电时,溶液中H+向PbO2电极移动 | |
| D. | 放电时,正极反应为:PbO2(s)+4H+(aq)+SO42-(aq)+2e-═PbSO4(s)+2H2O(l) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4 s(秒)时B的浓度为0.3 mol•L-1 | |
| B. | 4s内用物质A表示的反应速率为0.075 mol•L-1•s-1 | |
| C. | 达平衡后B的转化率为30% | |
| D. | 达平衡后若通入一定量氦气,A的转化率降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 14 | B. | 15 | C. | 13 | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀硫酸滴在银片上:2Ag+2H+=2Ag++H2↑ | |
| B. | 氧化铁与稀盐酸混合:Fe2O3+6H+=2Fe3++3H2O | |
| C. | 碳酸钙溶于醋酸溶液中:CaCO3+2H+=Ca2++CO2↑+H2O | |
| D. | 澄清石灰水与稀硝酸反应:Ca(OH)2+2H+=Ca2++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
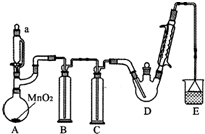 某探究小组设计如图所示装置(夹持、加热仪器略),模拟工业生产进行制备三氯乙醛(CCl3CHO)的实验.查阅资料,有关信息如下:
某探究小组设计如图所示装置(夹持、加热仪器略),模拟工业生产进行制备三氯乙醛(CCl3CHO)的实验.查阅资料,有关信息如下:| C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl | |
| 相对分子质量 | 46 | 147.5 | 163.5 | 64.5 |
| 熔点/℃ | -114.1 | -57.5 | 58 | -138.7 |
| 沸点/℃ | 78.3 | 97.8 | 198 | 12.3 |
| 溶解性 | 与水互溶 | 可溶于水、乙醇 | 可溶于水、乙醇、三氯乙醛 | 微溶于水,可溶于乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在常温下氮气比氧气和氯气稳定 | |
| B. | 氮、氧和氯的单质常温下为气体 | |
| C. | 氮、氧和氯分子在反应过程中释放能量 | |
| D. | 氮气、氧气和氯气的密度不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④⑥ | B. | ①②③⑤ | C. | ③④⑤⑥ | D. | 全部 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com