
【题目】下列说法正确的是( )
A.乙烯中![]() 键的键能是乙烷中
键的键能是乙烷中![]() 键的键能的2倍
键的键能的2倍
B.氧气分子中含有1个![]() 键和1个
键和1个![]() 键
键
C.![]() 键的极性比
键的极性比![]() 键的极性大
键的极性大
D.![]() 中4个
中4个![]() 键的键能不相等
键的键能不相等
【答案】B
【解析】
A.有机化合物中,碳原子与碳原子的原子轨道之间以“肩并肩”的方式形成![]() 键的重叠程度要比以“头碰头”的方式形成
键的重叠程度要比以“头碰头”的方式形成![]() 键的重叠程度小得多。两个碳原子之间形成的
键的重叠程度小得多。两个碳原子之间形成的![]() 键比
键比![]() 键牢固,
键牢固,![]() 键的键能大于
键的键能大于![]() 键。乙烯中两个碳原子间存在一个
键。乙烯中两个碳原子间存在一个![]() 键和一个
键和一个![]() 键,乙烷中两个碳原子间存在一个
键,乙烷中两个碳原子间存在一个![]() 键,乙烯中碳碳双键的键能应当大于乙烷中碳碳单键的键能且小于乙烷中碳碳单键的键能的2倍,故A错误;
键,乙烯中碳碳双键的键能应当大于乙烷中碳碳单键的键能且小于乙烷中碳碳单键的键能的2倍,故A错误;
B.氧气分子中氧原子与氧原子之间形成一个氧氧双键,包含1个![]() 键和1个
键和1个![]() 键,故B正确;
键,故B正确;
C.形成共价键的两个原子对电子的吸引能力差别越大,共价键的极性就越强,N原子与O原子吸引电子能力的差别小于C原子与O原子吸引电子能力的差别,所以![]() 键的极性比
键的极性比![]() 键的极性小,故C错误;
键的极性小,故C错误;
D.在![]() 中参与成键的8个电子分布在4个能量相等的
中参与成键的8个电子分布在4个能量相等的![]() 杂化轨道中,4个
杂化轨道中,4个![]() 键的键能、键长都相等,故D错误;
键的键能、键长都相等,故D错误;
综上所述,答案为B。


科目:高中化学 来源: 题型:
【题目】运用有关概念判断下列叙述正确的是( )
A.1mol H2燃烧放出的热量为H2的燃烧热
B.Na2SO3和H2O2的反应为氧化还原反应
C.![]() 和
和![]() 互为同系物
互为同系物
D.BaSO4的水溶液不导电,故BaSO4是弱电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钨是高熔点金属,工业上用主要成分为FeWO4和MnWO4的黑钨铁矿与纯碱共熔冶炼钨的流程如下,下列说法不正确的是( )
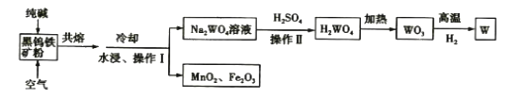
A.将黑钨铁矿粉碎的目的是增大反应的速率
B.共熔过程中空气的作用是氧化Fe(II)和Mn(II)
C.操作II是过滤、洗涤、干燥,H2WO4难溶于水且不稳定
D.在高温下WO3被氧化成W
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】决定物质性质的重要因素是物质结构。请回答下列问题:
(1)已知元素M是组成物质Ca5(PO4)3F的一种元素。元素M的气态原子逐个失去第1个至第5个电子所需能量(即电离能,用符号I1至I5表示)如表所示:
电离能 | I1 | I2 | I3 | I4 | I5 |
电离能/(kJ·mol-1) | 589.8 | 1145.4 | 4912.4 | 6491 | 8153 |
元素M化合态常见化合价是________价,其基态原子电子排布式为________________。
(2)Ca3(PO4)3F中非金属元素电负性由大到小的顺序为________________。
(3)PO43-的中心原子的杂化方式为________,该离子的空间构型为________,键角为________,其等电子体有________(请写出两种)。
(4)已知MgO与CaO的晶体结构相似,其摩氏硬度的大小关系为________,原因为__________________。
(5)CaF2晶胞结构如图所示,则CaF2晶体中与Ca2+最近且等距离的Ca2+数目为________;已知Ca2+和F-半径分别为a cm、b cm,阿伏加德罗常数为NA,M为摩尔质量,则晶体密度为________ g·cm-3(不必化简)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家最近在-100℃的低温下合成一种烃X,烃X分子的结构如图所示(图中的连线表示化学键)。下列说法正确的是( )

A.充分燃烧等质量的X和甲烷,X消耗的氧气较多
B.X是一种常温下能稳定存在的液态烃
C.X和乙烷类似,都易发生取代反应,不易发生加成反应
D.X既能使溴的四氯化碳溶液褪色又能使酸性KMnO4溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分。表中所列的字母分别代表某一种化学元素。

下列说法正确的是( )
A. 沸点A2D<A2X
B. CA3分子是非极性分子
C. C形成的单质中σ键与π键个数之比为1∶2
D. B、C、D形成的气态氢化物互为等电子体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A2+3B2 =2AB3在2L的密闭容器中进行,5s后,A2的物质的量增加了0.3mol,则此反应的平均速率可表示为:
A.v (A2)=0.01 mol/(L·s)B.v (B2)=0.08 mol/(L·s)
C.v (AB3)=0.03 mol/(L·s )D.v (AB3)=0.06 mol/(L·s )
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.![]() 的一溴代物和
的一溴代物和![]() 的一溴代物都有4种(不考虑立体异构)
的一溴代物都有4种(不考虑立体异构)
B.CH3CH=CHCH3分子中的四个碳原子在同一直线上
C.按系统命名法,化合物 的名称是2,3,4-三甲基-2-乙基戊烷
的名称是2,3,4-三甲基-2-乙基戊烷
D. 与
与 互为同分异构体
互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2是一种大气污染物,但它在化工和食品工业上却有广泛应用。某兴趣小组同学对SO2的实验室制备和性质实验进行研究。
(1)甲同学按照教材实验要求设计如图所示装置制取SO2
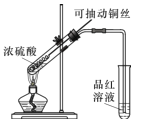
①本实验中铜与浓硫酸反应的化学方程式是 ______,铜丝可抽动的优点是_______。
②实验结束后,甲同学观察到试管底部出现黑色和灰白色固体,且溶液颜色发黑。甲同学认为灰白色沉淀应是生成的白色CuSO4夹杂少许黑色固体的混合物,其中CuSO4以白色固体形式存在体现了浓硫酸的________性。
③乙同学认为该实验设计存在问题,请从实验安全和环保角度分析,该实验中可能存在的问题是________。
(2)兴趣小组查阅相关资料,经过综合分析讨论,重新设计实验如下(加热装置略):

实验记录 A 中现象如下:
序号 | 反应温度/℃ | 实验现象 |
1 | 134 | 开始出现黑色絮状物,产生后下沉,无气体产生 |
2 | 158 | 黑色固体产生的同时,有气体生成 |
3 | 180 | 气体放出的速度更快,试管内溶液为黑色浑浊 |
4 | 260 | 有大量气体产生,溶液变为蓝色,试管底部产生灰白色固体,品红溶液褪色 |
5 | 300 | 同上 |
查阅资料得知: 产物中的黑色和灰白色固体物质主要成分为 CuS、Cu2S 和 CuSO4,其中CuS 和 Cu2S为黑色固体,常温下都不溶于稀盐酸,在空气中灼烧均转化为CuO和SO2。
①实验中盛装浓硫酸的仪器名称为 ____________。
②实验记录表明__________对实验结果有影响,为了得到预期实验现象,在操作上应该____________。
③装置C 中发生反应的离子方程式是 ___________________。
④将水洗处理后的黑色固体烘干后,测定灼烧前后的质量变化,可以进一步确定黑色固体中是否一定含有 CuS其原理为__________(结合化学方程式解释)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com