
分析 根据n=$\frac{V}{{V}_{m}}$计算HCl物质的量,根据m=nM计算HCl质量,溶液质量=水的质量+HCl质量,再根据V=$\frac{m}{ρ}$计算溶液体积,根据c=$\frac{n}{V}$计算溶液物质的量浓度.
解答 解:HCl物质的量为$\frac{aL}{22.4L/mol}$=$\frac{a}{22.4}$mol,HCl质量为$\frac{36.5a}{22.4}$g,溶液质量=(1000+$\frac{36.5a}{22.4}$)g,溶液体积=$\frac{(1000+\frac{36.5a}{22.4})g}{1000bg/L}$=$\frac{22400+36.5a}{22400b}$L,溶液物质的量浓度为$\frac{\frac{a}{22.4}mol}{\frac{22400+36.5a}{22400b}L}$=$\frac{1000ab}{22400+36.5a}$mol/L,
故答案为:$\frac{1000ab}{22400+36.5a}$mol/L.
点评 本题考查物质的量浓度有关计算,难度不大,注意掌握以物质的量为中心的计算.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 氯气作水杀菌消毒剂 | B. | 硅胶作袋装食品的干燥剂 | ||
| C. | 二氧化硫作纸浆的漂白剂 | D. | 铝热剂应用于焊接钢轨 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
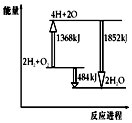
| A. | 拆开2molH2(g)和1molO2(g)中的化学键共吸收1368kJ能量 | |
| B. | 由H、O原子形成2molH2O(g),共放出1852kJ能量 | |
| C. | 1molH2(g)和$\frac{1}{2}$molO2(g)反应生成1molH2O(l),放出热量小于242kJ | |
| D. | 2molH2(g)和1molO2(g)反应生成2molH2O(g),共放出484kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 mol•L-1 | B. | 1 mol•L-1 | C. | 0.67 mol•L-1 | D. | 0.55 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 标准状况下,任何气体的摩尔体积都约为22.4 L | |
| B. | 1 mol气体的体积若是22.4 L,它必定处于标准状况 | |
| C. | 标准状况下,1molH2和O2混合气体的体积约为22.4 L | |
| D. | 标准状况下,11.2L水中含有分子的数目为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠着火,用水或CO2灭火器灭火 | |
| B. | 少量白磷保存在煤油中 | |
| C. | 不小心把水银洒落在地面,盖沙处理 | |
| D. | 硝酸银保存在棕色试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
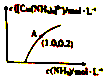 元素铜在溶液中主要以[Cu(H2O)4]2+(天蓝色)、[Cu(OH)4]2-(蓝色)、[CuCl2]-、[Cu(NH3)4]2+(深蓝色)等形式存在.CuCl为难溶于水的白色固体.回答下列问题:
元素铜在溶液中主要以[Cu(H2O)4]2+(天蓝色)、[Cu(OH)4]2-(蓝色)、[CuCl2]-、[Cu(NH3)4]2+(深蓝色)等形式存在.CuCl为难溶于水的白色固体.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com